日本国立研究开发法人原子能研究开发机构(JAEA)原子能基础工学研究中心的甲斐健师研究主干,与茨城大学研究生院理工学研究科的横谷明德教授、以及北海道大学研究生院保健科学研究院的松谷悠祐讲师、京都大学研究生院工学研究科的土田秀次副教授等共同发表成果称,明确了辐射致癌的起点——DNA损伤机制。通过模拟计算发现,即使在低剂量条件下,辐射分解水分子产生的电子和OH自由基同时与DNA发生反应,具有导致复杂的DNA损伤的可能性。这一发现有望为辐射防护策略提供科学支持。相关研究成果已发表在国际学术期刊《Communications Chemistry》的3月6日刊上。
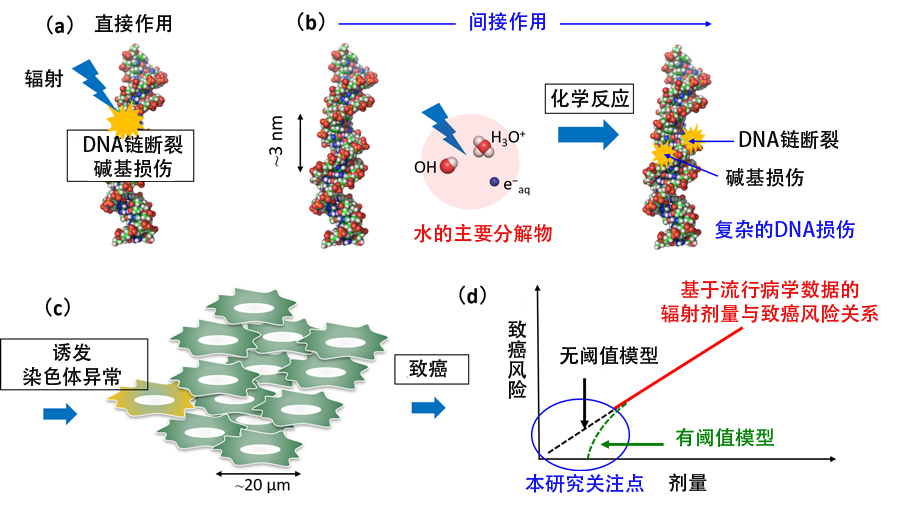
图1. 本研究探讨的辐射暴露致癌风险过程。(b)为本研究成果。(供图:JAEA)
由于辐射致癌的风险评估缺乏低剂量区间(100毫西弗)的流行病学数据,目前主要依赖模型推算。实验检测DNA损伤的技术尚未取得突破。另一方面,还存在“有阈值”和“无阈值”两种致癌剂量模型,此前学术界尚未明确哪种模型正确。
已有利用人工DNA的实验表明,DNA损伤作为致癌风险的初期因素,虽然这种损伤孤立存在时可被迅速修复,但若在10个碱基对范围内形成多重损伤(簇集损伤),修复蛋白对损伤部位的切除修复效果会下降。这将引发致癌风险。
此次研究团队聚焦于DNA附近生成的辐射分解物与DNA反应引发的间接损伤,对包含DNA的水溶液中H3O+、OH自由基、水合电子的随机扩散运动进行了计算。
本次研究假设一束辐射线在距离 x 纳米处击中 DNA,设定逸出电子(spur)的半径为α纳米,在此条件下计算了生成分解物的热扩散运动。然后评估生成分解物与DNA的化学反应。由此实现了对孤立损伤和簇集损伤产量的评估。
结果显示,当只有OH自由基与DNA反应时,将形成易修复的孤立损伤;而当OH自由基与水合电子同时与DNA反应时,将形成难修复的簇集损伤。关于簇集损伤,当在DNA极近旁(1.5纳米内)赋予水分子辐射能量并产生多个分解产物时,虽然发生概率不足1%(约为孤立损伤的1/50),但发现仍可能形成簇集损伤并致癌。
研究团队指出,此次研究结果为无阈值模型的观点提供了支持。
甲斐研究主干表示:“本次研究针对所谓低剂量辐射的影响展开,未来计划将研究拓展至癌症治疗等涉及的高剂量区域。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Communications Chemistry (Nature Portfolio)
论文:Multiple DNA damages induced by water radiolysis demonstrated using a dynamic Monte Carlo code
URL:https://www.nature.com/articles/s42004-025-01453-x