岐阜大学高等研究院的特任助教东小百合和德国明斯特大学的Seraphine V. Wegner教授等人组成的研究团队发表研究结果称,确立了控制巨型脂质体中金属酶活性的技术,并成功开发出了响应外部金属离子的刺激而改变命运的人造细胞。该技术将有助于设计模拟细胞分化的“多能性人造细胞”。相关研究成果已发表在国际期刊《Nature Chemistry》2024年12月23日刊上。
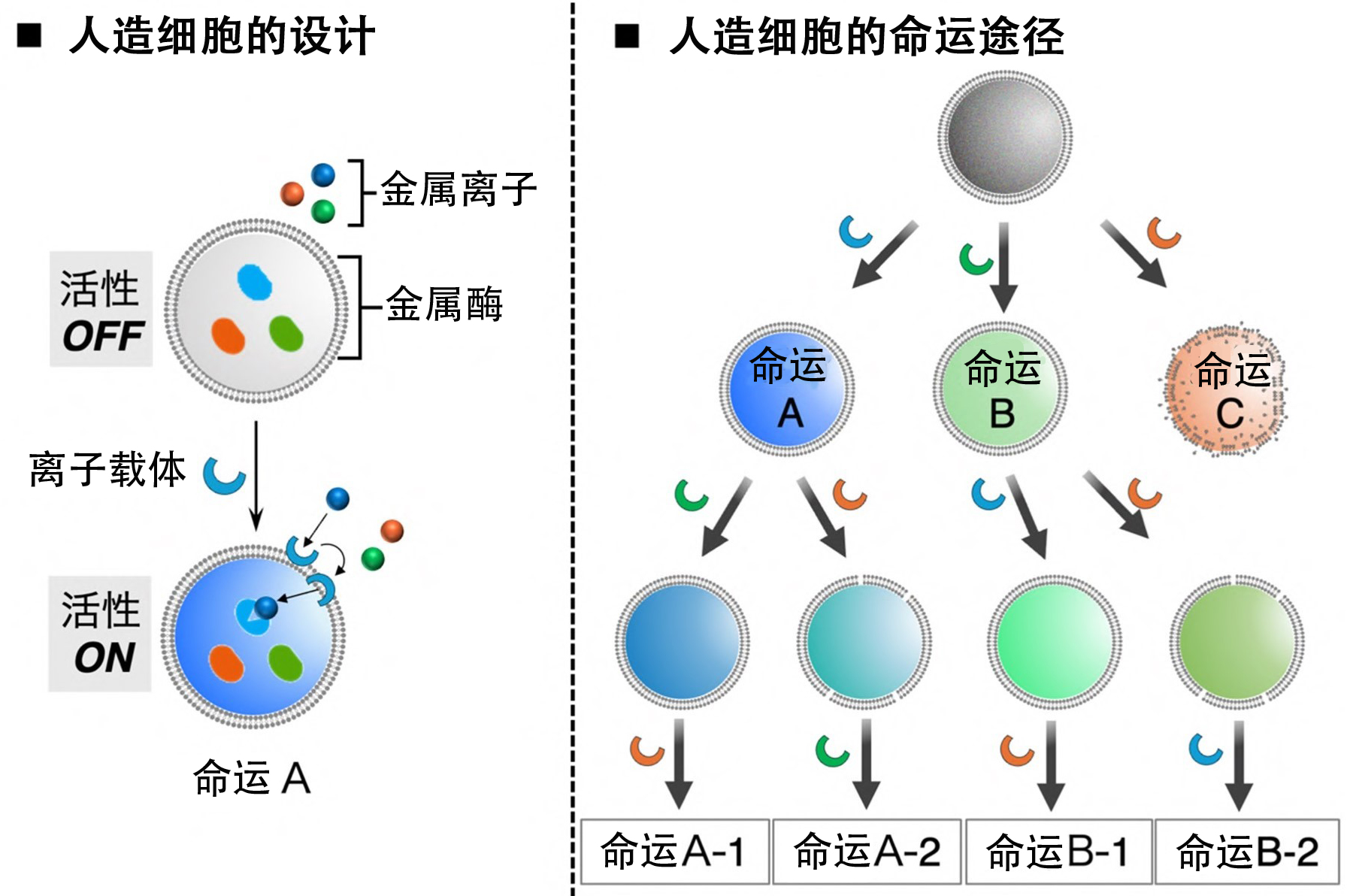
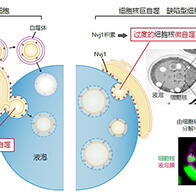
图1 研究概念图(供图:岐阜大学)
近年来,人们一直为了解细胞现象及其在生物材料中的应用而进行人工制造细胞的研究。为了模拟细胞的功能,人们开发出了如基因表达(复制、转录和翻译)、生成ATP(三磷酸腺苷)、由多种酶反应组成的新陈代谢、细胞分裂和融合、细胞间粘附和信息传递等具有重要基础功能的人造细胞。另一方面,大多数现有的人造细胞只注重于其中的一种功能,并被设计为响应外界刺激来表达功能。兼具多种功能的人造细胞此前一直未被开发出来。
另一方面,研究团队一直致力于开发巨型脂质体(GUV),并将其作为细胞膜来包裹生物分子,以此来进行开发人造细胞的研究。
此次,研究团队的目标是利用人造细胞来模仿细胞的适应性,开发出响应3种不同刺激的人造细胞。
在细胞中,将外部刺激正确传递到内部的机制非常重要,而在细胞膜上表达的转运体、通道和受体等膜蛋白会转运或结合不能通过细胞膜的物质,从而产生各种反应(细胞现象)。
因此,研究人员将向内部传递特定刺激的转运体与人造细胞膜结合,并将3种不同功能的金属依赖性酶封装在用作细胞膜模型的细胞大小的脂质体GUV内。通过与细胞膜结合的离子载体(提高特定金属离子的膜渗透性的分子群)所进行的金属离子转运来控制各种金属酶的活性。
事实证明,在人造细胞外部3种金属离子共存的环境中,将特定的离子载体结合到细胞膜上,会根据离子载体的选择表现出不同的功能。
研究还发现,同时将3种离子载体与细胞膜结合会同时抑制任一种金属离子的转运。
分子动力学模拟的结果表明,细胞膜内离子载体之间的相互作用可能会抑制它们在细胞膜上的移动,阻碍金属离子的转运。
此外,将3种离子载体按不同顺序与细胞膜结合后发现,与较晚结合到细胞膜上的离子载体相对应的金属酶的活性水平明显降低。由此可见,离子载体与细胞膜结合的顺序会影响金属酶的活性水平。
东特任助教表示:“该研究主要是我在德国明斯特大学韦格纳实验室留学期间进行的。在尝试利用巨型脂质体、金属酶和离子载体开发人造细胞模型的过程中,我经历了许多困难,也学到了很多。特别是将金属酶封装在巨型脂质体中时,花费了六个多月的时间才找到去除和灭活金属离子的最佳条件。未来,我希望利用金属离子相关的各种蛋白质,继续开发功能性人造细胞。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Nature Chemistry
论文:Adaptive Metal Ion Transport and Metalloregulation-Driven Differentiation in Pluripotent Synthetic Cells
DOI:10.1038/s41557-024-01682-y