北陆先端科学技术大学院大学物质化学前沿研究领域的都 英次郎教授及其研究团队发表研究成果称,成功制造出了在碳纳米管之一的碳纳米角(CNH)表面包覆癌细胞成分和抗癌药物的纳米粒子,并在小鼠身上证实了这种粒子不仅具有纳米粒子特有的高渗透长滞留效应(EPR效应),还能发挥对多种癌症的治疗作用。这种粒子对机体的影响极小,有望创造出纳米粒子与近红外激光相结合的新型癌症诊断和治疗技术。相关研究成果已于8月19日发表在国际学术期刊《Small Science》上。
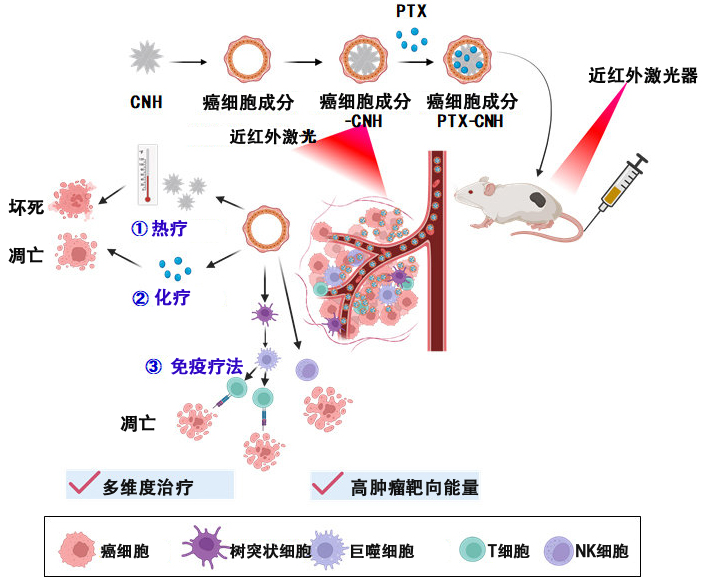
图1 包覆癌细胞成分的纳米粒子的制造过程及其研究概念。(供图:北陆先端科学技术大学院大学)
已知癌细胞有躲避免疫细胞攻击的特殊细胞膜功能,且癌细胞内的组成成分(基因和蛋白质等)具有增强免疫活性的作用。
都教授此前发现,CNH不仅具有较高的生物相容性和优秀的物理化学特性,还具有在生物渗透性较高的波长区域(650~1100纳米)的激光照射下容易发热的特性,因此一直致力于开发利用这一特性的癌症诊断和治疗技术。
另一方面,CNH具有因分子间相互作用较强而难以在水等介质中分散,从而聚集的性质。该问题可通过在CNH表面化学修饰聚乙二醇(PEG)等水溶性聚合物来解决,但这种方法存在反复给药导致血液滞留性丧失和引发过敏反应的问题。
此次新开发的技术通过操作简便的超声波照射,使癌细胞成分吸附在CNH表面,从而使CNH能够分散在水溶液中。此外还通过利用癌细胞成分,成功地将难溶于水的抗癌药物“紫杉醇(PTX)”同时包覆在了CNH表面。
研究证实,通过该方法制备的癌细胞成分-PTX-CNH复合物可保持粒径稳定性超过30天,对细胞具有较高的细胞膜渗透性,并表现出了抗癌效果。研究还证实该物质在近红外激光照射下会发热,由此进一步验证了该技术在癌症病灶的可视化与治疗效果的潜力。
在癌症病灶的可视化方面,研究团队利用了一种将可用于癌症诊断的近红外荧光色素“吲哚菁绿(ICG)”与癌细胞成分一起结合到CNH表面的纳米粒子(癌细胞成分-ICG-CNH复合物)。
当研究人员向移植大肠癌后约10天的小鼠投用癌细胞成分ICG-CNH复合物,并在24小时后用近红外光(波长740-790纳米)照射后,结果得到了癌症病灶发出荧光的图像。
用波长为808纳米的近红外激光照射癌细胞成分-ICG-CNH复合物聚集的病灶后,研究发现,在癌细胞成分产生的血液滞留效应、肿瘤内浸润作用、免疫激活能力、抗癌药物产生的药效,以及CNH的光热转换产生的效果的联合作用下,成功在两天后完全消除了癌症。
此外,进一步研究肿瘤内部的药效机制时发现,激光照射后癌细胞成分-ICG-CNH复合物中,细胞毒性较高的T细胞和自然杀伤(NK)细胞等免疫细胞被激活。
都教授表示:“此次开发的技术的特点是将癌症的靶向疗法、光热疗法、化疗和免疫疗法等多种疗法的优势整合在了一个平台上,我们希望它能为癌症治疗,特别是转移性癌症的治疗提供一种有效且精准的方法。此外,我们也在积极开展安全性试验等方面的研究,目标是在10年内开展临床试验。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Small Science
论文:Biomimetic functional nanocomplexes for photothermal cancer chemo-immunotheranostics
DOI:10.1002/smsc.202400324













