熊本大学发育医学研究所的古贺沙绪里助教和小川峰太郎教授的研究团队发表研究成果称,成功在试管中将造血干细胞的祖细胞——血管内皮细胞诱导分化成为了造血干细胞。研究团队通过再现由血管内皮细胞分化造血干细胞的发育过程所需环境,获得了上述成果。由于无需基因改造或添加血清等,这种方法具有高的通用性,因此有望成为明确造血干细胞发育的详细机理的强大工具。相关成果已发表在《美国国家科学院院刊》(PNAS)7月23日号上。
造血干细胞存在于骨髓中,能够不断自我复制并产生血液细胞。如果这些细胞出现问题或发育过程中发生基因异常,则会导致血液病。
因此,如果能在试管中再现造血干细胞的正常发育过程,将有望通过研究基因突变的影响揭示疾病的原因。
另一方面,既往研究中在试管中从血管内皮细胞分化造血干细胞时,需要与经过基因改造的支持细胞共同培养,或在有血清存在的情况下培养。但由于这种方法通用性较低及血清中细胞因子等的影响,阻碍了解明机制的进程。
本次研究人员旨在克服这些问题,构建一种仅使用通用材料的无血清造血干细胞分化诱导方法。
造血干细胞是胚胎期主动脉内的血管内皮细胞通过前造血干细胞发育而成的。
研究人员在小鼠胚胎体内探索了前造血干细胞表达的信号因子受体,并发现其中表达了SCF(干细胞因子)受体KIT和TPO(血小板生成素)受体MPL。
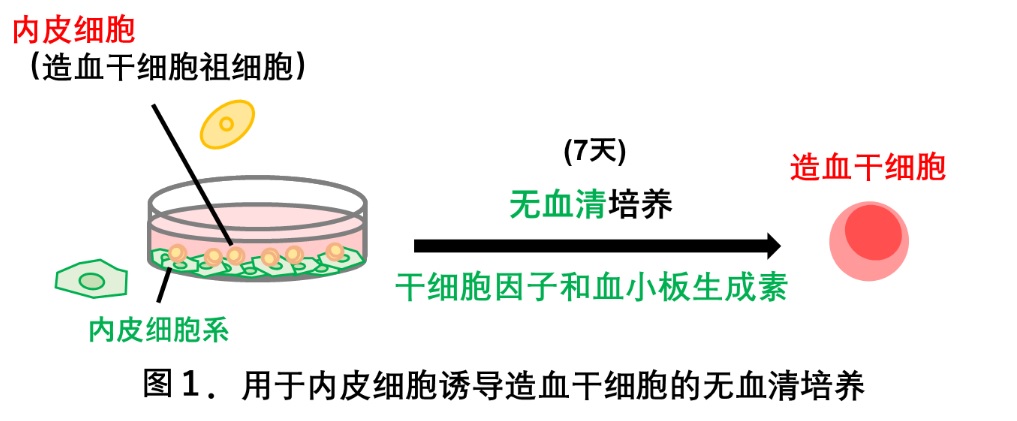
在无血清培养液中培养前造血干细胞时,研究人员通过添加SCF和TPO,使其分化为了造血干细胞,而单独添加任何一种都不会导致分化。
研究团队进一步探索了血管内皮细胞分化为造血干细胞的条件。结果发现需要添加血管内皮细胞株作为血管内皮细胞的支持细胞。
胚胎体内血管内皮细胞发育的主动脉腔内存在SCF,但不存在TPO。
由于TPO只由肝母细胞产生,研究发现,前造血干细胞从主动脉腔内迁移到肝脏后,接受TPO信号后才能分化为造血干细胞。
古贺助教表示:“本研究中确立的培养方法只使用了全球研究人员都能简单获取的研究工具,因此有望成为详细研究造血干细胞发育过程的标准方案。 今后,我们的目标是建立从多能干细胞到造血干细胞发育过程的再现培养技术。并将致力于开展能够对医学领域做出贡献的研究,如再生医学的应用和疾病原因的阐明等”。
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Proceedings of the National Academy of Sciences of the United States of America (PNAS)
论文:Transition of signal requirement in hematopoietic stem cell development from hemogenic endothelial cells
DOI:10.1073/pnas.2404193121













