
检测时间从3个半小时缩减至5分钟
为超早期癌症的无痛诊断开辟道路
近年来,肿瘤学领域正在加速向精确掌握癌症患者的病理变化,并将其反映到治疗方案中的精准医疗方向发展,在开发治疗药物的同时,开发能够检测微量生物标志物的先进检查方法也变得越来越重要。作为微量生物标志物,包含mRNA等的纳米微粒“外泌体”(Extracellular vesicle、EV,细胞外囊泡)最为受人关注。从微量样品中快速灵敏地检测出纳米级EV,对于癌症等难治性疾病的早期诊断非常有用。但是,既往的检测方法通常需要数小时的超离心分离等复杂流程。
大阪公立大学LAC-SYS研究所所长饭田琢也、副所长床波志保、所长助理中濑生彦等人组成的研究团队2023年发表了一项令人瞩目的成果。英国皇家化学会发行的《Nanoscale Horizons》是业界非常权威的科学杂志之一,饭田等人的这篇论文入选了该杂志的“2023 Outstanding Paper Award”表彰,受到了国内外的高度评价。
此项研究省略了超离心分离等的复杂流程,将来自癌细胞的纳米微粒EV的检测时间从3个半小时缩短到了5分钟。其具体做法是,在激光照射下产生光诱导力,加速EV和与EV表面膜蛋白质选择性结合抗体“抗体修饰珠”的结合反应(图1),并利用可实现高分辨率和三维信息重建的“共焦光学系统”分析了由上述结合反应聚集的微粒立体结构。
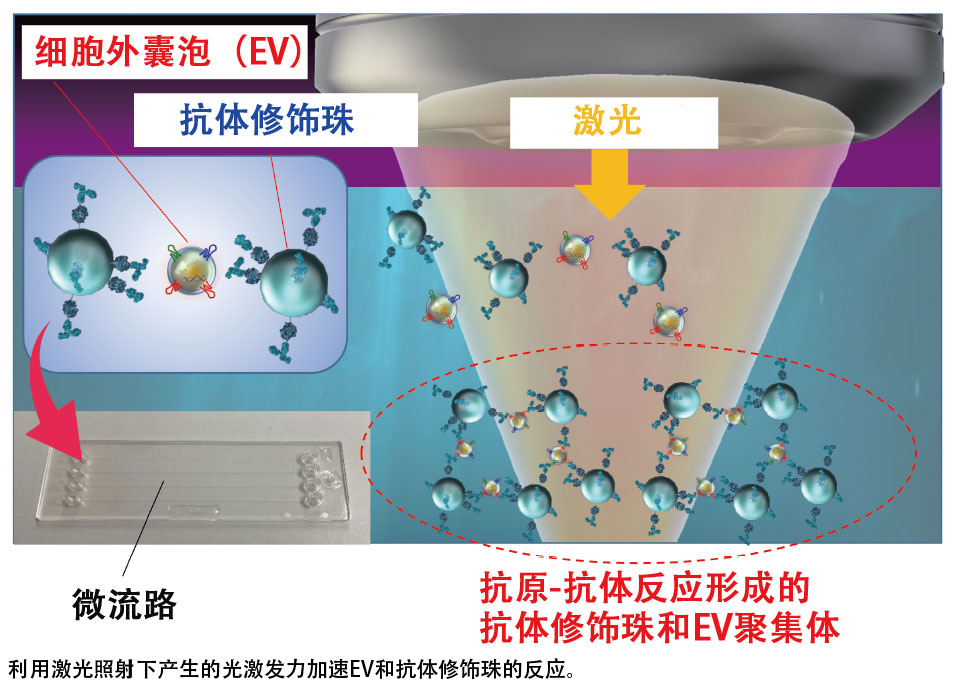
图1细胞外囊泡的微流光浓缩概念图
研究结果显示,仅花费5分钟便成功在500纳升(纳升是10亿分之1升)样本中检测出了约1000~10000个纳米级EV。能够检测的EV量相当于既往方法的4000分之1,可检测出极微量的样本。此外,研究团队还成功检测出了大肠癌细胞和肺癌细胞分泌的EV表面的状态差异。饭田教授介绍说:“应用该技术甚至能对芝麻粒大小的微量血液进行检测,实现既往方法难以实现的超早期无痛癌症诊断,这将有助于癌症的治疗。”
浓缩生物质以加速反应
利用发热效应的新原理
为了进一步提升此前的研究成果,饭田教授等发明了“光浓缩”技术。这是一种利用光激发力以及由光发热产生的光激发对流的协同效应来浓缩生物质并加速反应的方法。这一想法来源于“光镊”通过透明物体和周围液体之间折射率的差异产生光激发力,从而将物体吸引到光线强区域的技术。通过将激光聚光到与光的波长相同程度的衍射极限,提高所产生的光的压力,从而捕获和操纵细胞等数微米(微米为百万分之一米)以下的微粒的技术。
饭田教授等研究人员在世界上首次证实了光浓缩原理,通过在光激发力捕获的金属纳米微粒周围产生对流和气泡,实现了靠对流搬运来的微粒在气泡表面的聚集。研究团队利用该原理,在几分钟内成功检测出了1万亿分之一克的微量蛋白质,并于2014年发表了论文。之后在JST的未来社会创造事业项目中继续推进研究,在和人的血管相似粗细的流道中,利用泵的压力和光的压力使金属纳米微粒高效聚集,再通过集合体产生的热效应实现了气泡产生的高效率化。
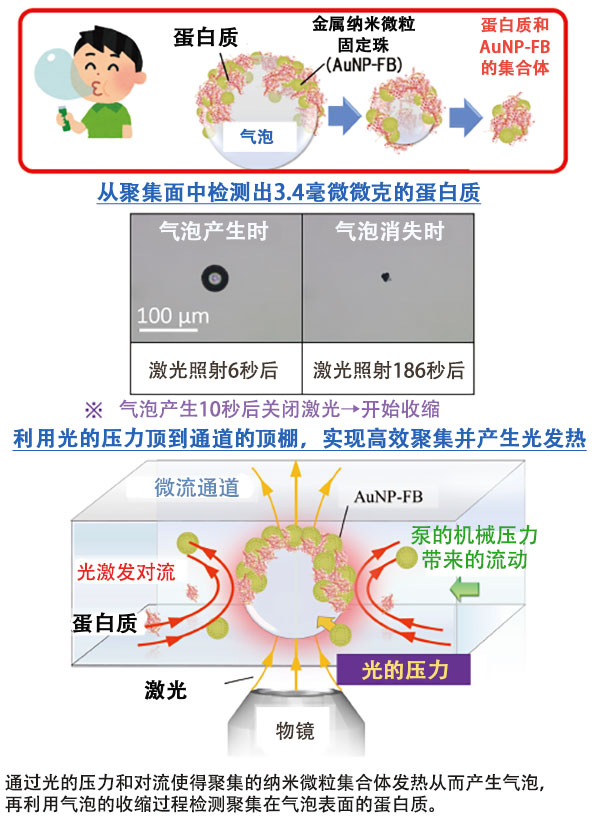
图2可以检测1毫微微克量级的蛋白质的“泡泡糖传感器”
研究团队将这样生成的气泡用于在通道中的收缩过程,开发出了在几分钟内从吸附在气泡表面的蛋白质和金属纳米微粒的集合体中检测出1毫微微(毫微微为千万亿分之一)克量级蛋白质的“泡泡糖传感器”(图2)。这种传感器将成为生物分析技术的基础,能够以高出早期试验1000倍以上的高灵敏度从微量体液中检测出引发成人病等疾病的蛋白质。该研究成果可以为食品行业和医疗领域提供全新的检测方法,后续开发可通过控制发热量,使其能够应用于耐热性较差的EV。(未完待续)(TEXT:伊藤左知子;PHOTO:石原秀树)
原文:JSTnews 2024年7月号
翻译:JST客观日本编辑部














