京都大学开发了一种只在目标细胞中使基因发挥作用的基础技术。由于治疗时基因只作用于癌细胞等异常细胞,因此有望减轻治疗的副作用。此外,还有望降低使用免疫细胞进行治疗的成本。目标是在2050年代作为新一代基因疗法普及应用。
京都大学iPS细胞研究所(CiRA)的齐藤博英教授等通过识别细胞内的分子,开发出了基因仅在特定细胞中发挥作用的特殊蛋白质。相关研究成果已发表在英国科学杂志《自然通讯》上。
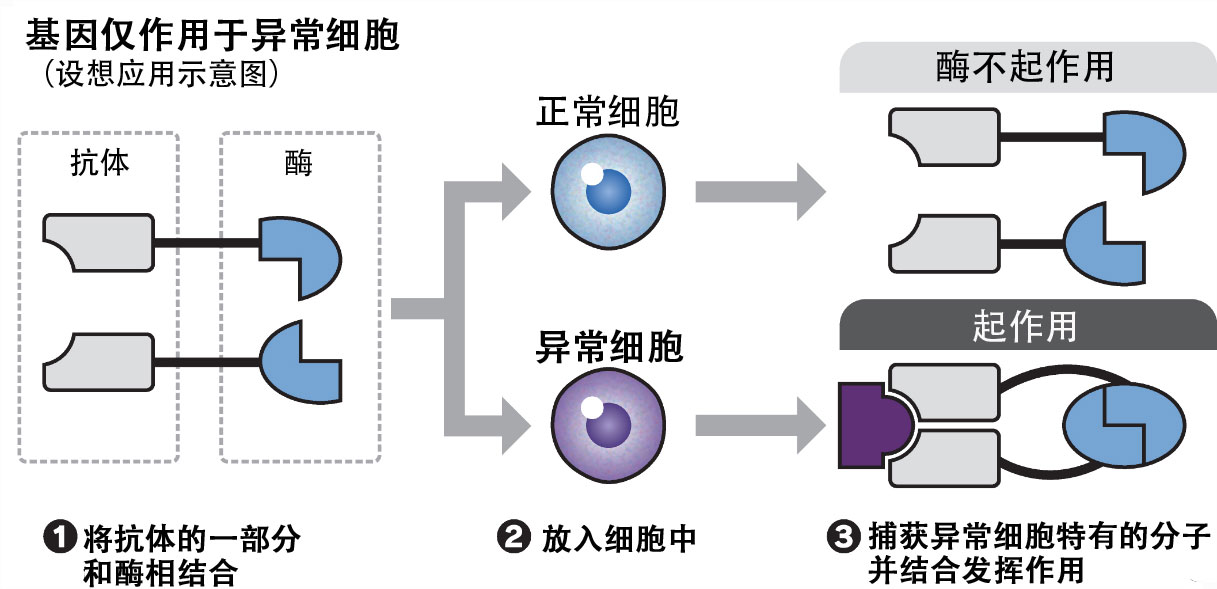
开发的蛋白质由从DNA合成RNA(核糖核酸)的名为“聚合酶”的酶和抗体的一部分结合后而成,共2对,只有结合在一起后,治疗用基因才会表达。由于结合需要特定细胞内所含的分子,因此基因很难在正常细胞中发挥作用。理论上可以减少治疗性蛋白质在健康脏器中的积累等副作用。
不同的细胞内部存在的分子也各有差异。所以,当细胞发生癌变时,就会随之产生正常细胞中不存在的异常分子或蛋白质。目前通过检测这些分子和蛋白质实现癌症早期诊断的研究正在推进之中。
本次研究通过利用生物体内的这一现象,设想只用治疗用基因攻击癌细胞,从而抑制肿瘤生长的使用方法。传统化学疗法的抗癌药物也作用于正常细胞,会给人体造成一定程度的伤害。如果能够做到只攻击癌细胞,就可以减轻副作用。
此次开发的技术,只要改变与特定分子结合的抗体类型,就还可应用于癌症治疗以外的领域。比如,利用抗体可以区分由多个氨基酸相连组成的肽、蛋白质和RNA等各种分子构造上的差异。
通过改变用于治疗的基因类型,不仅可以产生蛋白质,还可以产生“基因编辑”修改细胞基因所必须的RNA。
研究团队认为该技术可应用于将T细胞(一种免疫细胞)进行基因修改让其攻击癌细胞的“CAR-T细胞疗法”。
“Kymriah”和“Yescarta”等获得药事批准的治疗药物价格均在3000万日元以上,非常昂贵。因为这些目前的CAR-T细胞疗法是从患者体内取出T细胞,进行基因修改后再返回体内的缘故。
而利用此次开发的技术,将有可能在患者体内仅对T细胞进行基因修改。由此可以减少体外管理细胞所需的时间和成本。
此次开发的技术用于临床时,是否能够真的发挥作用,以及是否存在安全问题等是今后必须解决的课题。
此外,该技术还有望应用于在由iPS细胞生产治疗用细胞时从中仅选择出高质量的细胞,或识别被病毒感染的细胞等。负责该项研究的研究生小松将大介绍说:“该技术的应用范围非常广泛”。
同时推进基础研究

操作基因工作方式的基因表达控制技术有助于生命现象的阐明。其不仅可用于开发疾病治疗方法等临床应用,还有望推进基础研究。
传统研究很多都是采用人体拥有的控制系统来进行的。而此次开发的技术灵活应用带有病毒的酶等,因此有望创建出对人体内部系统难以产生不良影响的灵活机制。
然而,要想成为可以自由操纵基因功能的便利工具,还有需要解决的课题,也即目前开发的蛋白质还相对较大。一般来说,抗体等大分子很难通过细胞表面的细胞膜。为此,研究人员正在考虑将抗体和酶包裹在脂质膜中,或将想要利用的基因加到无害的病毒上使其进入细胞内。
使用脂质和无害病毒的方法已经被用于制作新冠病毒疫苗。重要的要让被吸收的蛋白质在细胞内有效地发挥作用。推进来自基础研究的方法,也是扩大该技术应用范围的关键。
日文:尾崎达也、《日经产业新闻》、2023/11/24
中文:JST客观日本编辑部













