北海道大学遗传病控制研究所癌症控制学领域的园下将大教授等人组成的研究团队发布研究成果称,制作了模仿胰腺癌患者中观察到的4个基因突变的胰腺癌模型果蝇,并通过全面筛查成功找到了新的治疗靶点。研究人员还在果蝇(4-hit果蝇)中成功再现了4个基因突变,通过利用这种果蝇对所有激酶进行全面的基因筛查,找到了新的治疗靶点,并证实了这种抑制剂可以提高4-hit果蝇的存活率。这一发现有望促进胰腺癌治疗药物的开发。研究成果已发表在美国癌症协会杂志《Cancer Research》6月28日号上。
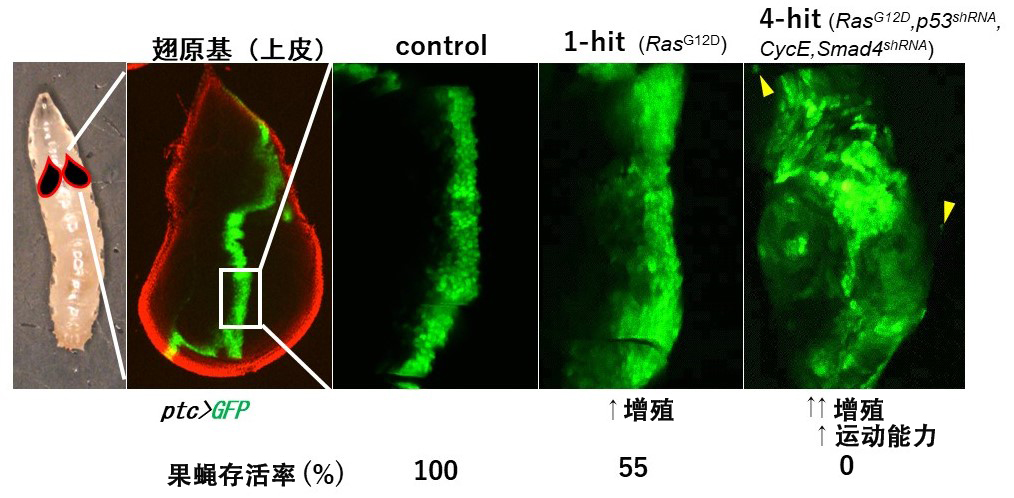
图 胰腺癌基因型果蝇模型中的肿瘤发生。利用patched (ptc) 基因启动子活性驱动GFP表达,标记幼虫翅原基的单层上皮细胞。在“1-hit”果蝇中,Ras基因的激活诱导细胞增殖。此外,改变4个基因的“4-hit”果蝇表型恶化并产生迁移细胞(箭头),出现致死现象。(供图:北海道大学)
胰腺癌是治疗选项极为有限的难治性癌症之一,癌基因KRAS的活化和抑癌基因组TP53、CDKN2A和SMAD4的失活可单独或组合出现。同时具有这4个基因突变的患者预后最差,但目前尚无再现该病况的模型小鼠,新模型动物的制作备受期待。
果蝇携带超过70%的人类疾病中观察到的异常基因,与哺乳动物具有高度的遗传保存性,以及对应功能的体内构造。
2019年,上述研究团队利用将甲状腺髓样癌基因突变导入果蝇的模型蝇进行了基因筛查和化合物筛查,发现了可作为新治疗靶点和候选治疗药物的激酶抑制剂。
此次,研究团队在世界上首次成功制作出再现胰腺癌中出现的4个基因突变的模型果蝇(4-hit果蝇),并通过单独或组合方式在幼虫翅原基中再现了与人类各基因对应的果蝇基因的活化和功能减弱。
首先,研究人员制作了在幼虫的翅原基上皮细胞中仅激活果蝇Ras基因(人类为KRAS基因)的1-hit苍蝇,并分析了表现型。观察到细胞增殖加速,约有一半的个体死亡。此外,进一步制作了4-hit果蝇,观察到翅原基上皮细胞的增殖和游走能力明显增强,并且在未羽化之前全部死亡。这些结果证实,果蝇能够毫无矛盾地反映临床胰腺癌的病况。
其次,研究人员使用4-hit果蝇对所有激酶进行了全面的基因筛查。大多数癌症中都发现了激酶的异常,并且被认为与癌症中异常细胞的增殖密切相关。在该分析中,针对4-hit果蝇,研究人员一一制作了缺乏果蝇激酶基因功能的系统,并分析了对病况带来的变化。据称,人类大约有500个激酶基因,而果蝇的数量大约是人类的一半。
结果发现,降低MEK和AURKB的活性后,可提高4-hit果蝇的存活率。
于是,研究人员进行了将MEK抑制剂(Trametinib,曲美替尼)和AURKB抑制剂(BI-831266)作为抑制激酶活性的化合物经口给予4-hit果蝇的实验。
实验结果表明,与单剂给药相比,2剂的组合给药更有助于恢复4-hit果蝇的存活率。并且确认,即使在植入人类胰腺癌细胞的模型小鼠中,2剂给药也能明显抑制肿瘤的生长。此外,对北海道大学医院胰腺癌患者手术样本的分析显示,存在磷酸化组蛋白H3(AURKB活化指标)的患者组的预后比没有磷酸化组蛋白H3的患者组更差。
据该研究团队称,已经发现了多个其它的候选新型治疗靶点。
园下教授表示:“此次的研究成果揭示了基于果蝇表达系统筛选的药物研发的可能性。在哺乳动物中很难实现的实验,但可以在果蝇中有效地进行,相信这种方法也可以应用于胰腺癌以外的其他癌症。未来将在努力研发胰腺癌治疗药物的同时,还将尝试掌握与胰腺癌发病相关的信号通路的整体情况。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
杂志:Cancer Research
论文:Drosophila screening identifies dual inhibition of MEK and AURKB as an effective therapy for pancreatic ductal adenocarcinoma
DOI:doi.org/10.1158/0008-5472.CAN-22-3762













