随着肥胖的增加,全球范围内因胆固醇过度累积而患上非酒精性脂肪性肝病(nonalcoholic fatty liver disease,NAFLD)的患者数量不断在增加,部分NAFLD会发展为以炎症和纤维化为主要特征的非酒精性脂肪性肝炎(nonalcoholic steatohepatitis,NASH)。日本也是如此,随着生活方式的西化,体检诊断出NAFLD的患病率为9~30%,其中约10%被推定为NASH。10~20%的NASH患者会出现肝硬化和肝癌。然而,由于导致NASH形成的因素尚未完全阐明,因此除了饮食和运动疗法外,尚无有效的治疗方法。
京都大学研究生院医学研究科循环器内科的尾野亘教授、堀江贵裕助教在对miRNA进行功能分析的过程中发现,肝细胞的miRNA-33b(miR-33b)在NASH形成中发挥着重要作用。此外,还发现通过投喂特异性抑制33b的合成核酸,可以抑制NASH小鼠模型的炎症、纤维化和肝损伤,表明这种核酸药物可用于治疗NASH。尾野教授表示:“今后将继续开发以应用于实际治疗”。该研究成果已发表在《Life Science Alliance》上。
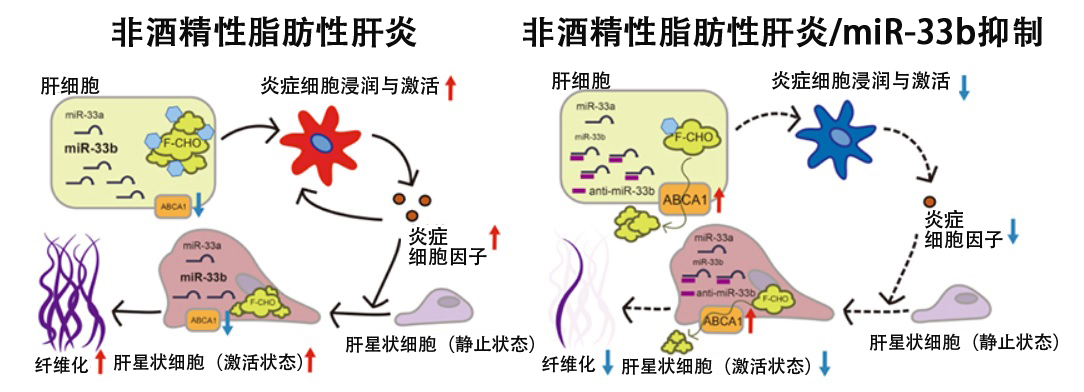
图1 肝细胞和肝星状细胞中miR-33b的表达高于miR-33a,通过投喂anti-miR-33b,肝细胞及肝星状细胞的ABCA1表达上升,且通过减少这些细胞内游离胆固醇和肝内胆固醇结晶,减轻了肝脏炎症反应和纤维化。因此,肝细胞和肝星状细胞中的miR-33b对于NASH发病具有重要作用,抑制miR-33b有望成为新的NASH治疗方法。(供图:京都大学)
研究团队此前已明确,小鼠的miRNA-33可抑制细胞内胆固醇转运蛋白ABCA1的表达。ABCA1将胆固醇从细胞内输送到细胞外,形成好胆固醇。因此,激活miRNA-33会抑制ABCA1并降低好胆固醇。实际也已确认缺失miRNA-33的小鼠的动脉硬化和主动脉瘤的形成受到了抑制。
小鼠体内的miRNA-33只有1种,而人体内则有2种,为此将与小鼠位于同一位置的命名为a,另一个命名为b。33b的作用尚不明确。
研究团队制作了人源化基因敲入小鼠,并在与人类相同的位置插入了33b。这种小鼠中,33a和33b均有表达,且与野生型相比,动脉硬化加剧。
对小鼠肝脏的整体脂质分析表明,表达33a的小鼠脂质较多,而同时表达33a和33b的基因敲入小鼠具的脂质更多。
当给基因敲入小鼠投喂高脂肪食物后发现,脂肪在肝脏中累积,并伴有炎症和纤维化,以及表现出NASH症状。此外,肝脏中的胆固醇和甘油三酯过度累积。相反,使肝细胞特异性缺失33b后,NASH表达型得到改善,而使巨噬细胞特异性缺乏33b也没有改善表达型。堀江助教表示:“我们发现,给基因敲入小鼠投喂高脂肪饮食可使其成为NASH模型小鼠。”
接着,研究人员在生物体中制备了能单独抑制33a/b的人工核酸,连续12周投喂NASH诱发食物,同时每2周1次向基因敲入小鼠皮下注射抑制33a的人工核酸、抑制33b的人工核酸,及抑制33a/b的人工核酸。
在21周龄时确认给药效果后发现,在对照组中观察到小鼠肝脏中胆固醇累积,炎症细胞浸润,细胞因子增加,肝星状细胞活化和纤维化进展,而与此相对照,皮下注射人工核酸的小鼠胆固醇累积受到抑制。特别是,对肝脏中高表达的33b显示出明显抑制效果,甚至与同时抑制a和b的情况相比,对炎症细胞因子和纤维化基因的抑制更多。
堀江助教表示:“通过此次的实验,我们发现人源化miR-33b基因敲入小鼠表现出NASH,其中肝细胞的miR-33b尤为重要。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
杂志:Life Science Alliance
论文:Inhibition of microRNA-33b in humanized mice ameliorates nonalcoholic steatohepatitis
DOI: 10.26508/lsa.202301902













