CRISPR-Cas9作为一种可以自由编辑各种细胞的靶向基因的革新性技术,极大地推动了基础研究的发展,同时在医学领域的应用也备受期待。然而,传统方法无法避免由过度切割基因组引发的非目标基因组位点的脱靶突变和细胞毒性等风险。九州大学生体防御医学研究所的川又理树助教、木村亮太(研究当时为硕士研究生)、铃木淳史教授以及名古屋大学大学院医学系研究科的铃木洋教授组成的共同研究团队开发出了一种可自由微调基因组切割活性的新技术,成功构筑了能将安全性和准确编辑效率提高数百倍的新一代基因编辑平台。川又助教表示:“这项技术可以精确控制DNA的切割与否。已经证实了可以应用于Cas9以外的领域,目前美国成立初创公司(One Genomics, Inc.)正在推进其实用化进程。”研究成果已发表在《Nature Biomedical Engineering》杂志上。
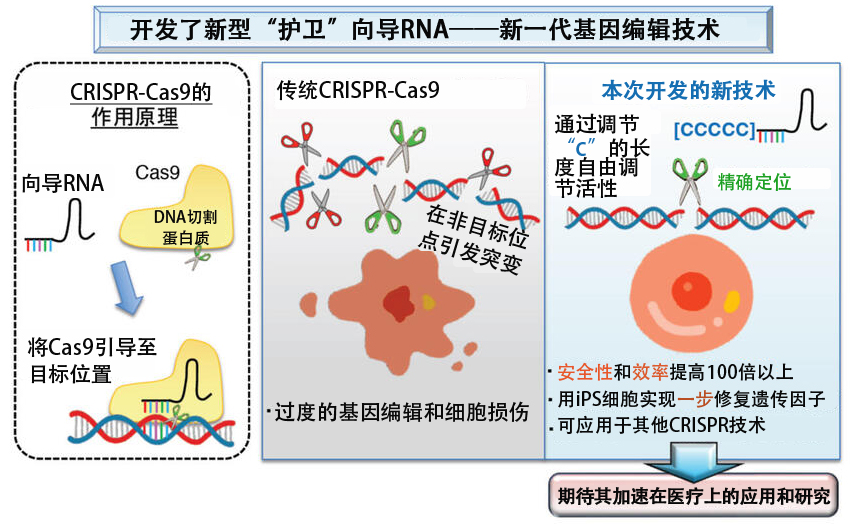
图:此次开发的基因编辑新技术概念图(供图:九州大学)
虽然CRISPR技术在海外已用于基因治疗,但由于现有的CRISPR工具尚未针对人类细胞基因编辑进行优化,因此在接受CAR-T癌症治疗的患者中出现了染色体易位现象,接受肌肉萎缩症治疗的患者中也出现了死亡案例。
川又助教等人此前曾错误设计DNA亲和力较弱的gRNA(向导RNA)时,根据有效获得精确编辑细胞的经验,认为按照现有的编辑方案,Cas9的DNA切割活性过剩,从而导致了各种问题的产生,所以决定开发可自由调节Cas9活性的新技术。
研究团队首先在小鼠ES细胞上构建了可以通过荧光标记分别评估来自父母染色体的Cas9活性(随机碱基插入或缺失)的AIMS系统(Allele-specific Indel Monitor System)。通过AIMS测量使用常规gRNA时的Cas9活性,发现99.4%发生了基因缺失或随机插入。
通过使用AIMS,研究人员探索了能够抑制Cas9高活性的gRNA修饰方法,发现在5'端添加多个额外的胞嘧啶可以起到抑制过度活性的作用。胞嘧啶链越长,gRNA:Cas9复合体与靶DNA的结合能力(亲和力)就越低,切割能力也越低,细胞内摄取的gRNA量也越少。由此开发出一种通过调整胞嘧啶链的长度便可以阶段性地抑制Cas9活性的非常简便的精细调节系统——护卫gRNA。
研究人员分析了阶段性抑制活性对单个等位基因编辑模式、同源重组修复(HDR)介导的精确编辑效率以及细胞毒性平衡的影响。结果表明,可以避免细胞毒性,提高从两个等位基因中选择一个进行编辑的效率,并且可以抑制脱靶,从而大幅提高HDR的效率。此外,这些效果可以获得非HDR等位基因无损伤的报告基因等敲入细胞,实现一步即可完成单等位基因1碱基的编辑以及制作和修复异型SNP疾病模型。
异型SNP疾病模型的基因组编辑是一种难度极高的基因编辑技术,它需要在两个具有相似序列的基因组等位基因中,仅对其中一个等位基因导入1碱基的突变,而另一个等位基因保持不变。事实上,研究人员已成功制备出能忠实再现发病率为200万分之一的超罕见疾病(FOP)基因型胚胎干细胞小鼠模型。此外,他们还能够在FOP患者来源的iPS细胞中精确修复导致疾病的等位基因SNP,展示了其作为安全高效基因治疗法的潜在价值。
同时,通过结合AIMS和大规模实验数据以及数学模型,研究人员首次成功揭示了对于如单碱基替换的精确编辑等各种基因组编辑用途所需的最佳Cas9活性及其规律。这使得在各种基因组编辑实验中,可以根据不同的目标模拟最佳的Cas9活性,通过使用最佳的护卫gRNA,实现最安全、有效的基因组编辑。
另外,研究人员还证实了护卫gRNA不仅适用于Cas9,还适用于Cas12a(Cpf1)以及CRISPRa/i(激活/干扰)等基因组和表观基因组的编辑调控。
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
杂志:Nature Biomedical Engineering
论文:Optimization of Cas9 activity through the addition of cytosine
extensions to single-guide RNAs
DOI:10.1038/s41551-023-01011-7













