筑波大学教授山崎聪和庆应义塾大学的专任讲师樱井政寿等宣布开发出了在体外培养红血球等血液细胞来源的人体造血干细胞技术。研究人员将脐带血中的造血干细胞进行为期一个月的培养,使其数量得以增加。如果能有效确立增加治疗白血病等时移植用造血干细胞的技术,那么就有望实现安全的移植以及解决供体(捐献者)短缺的问题。
经过培养的人体造血干细胞(供图:筑波大学山崎教授)
该技术是筑波大学、庆应义塾大学与东京大学、美国斯坦福大学、盐野义制药株式会社及德国巴斯夫集团(BASF)共同开发的。造血干细胞存在于骨髓和脐带血中,是产生红血球、白血球、血小板等各种血液细胞的源泉。2019年,山崎教授等通过在培养液中加入液体胶的主要成分聚乙烯醇(PVA),成功地在体外增加了小白鼠的造血干细胞的数量。此次进一步将该技术应用到了人体造血干细胞上。
此前需要在培养液中加入名为“细胞因子”的蛋白质,此次则替代为复数中化合物,脐带血中的造血干细胞在一个月内获得了稳定培养,并且增加了数量。此外,研究团队还发现当使用BASF开发的用于药物添加剂的高分子化合物代替PVA时,增殖效率会提高。利用该方式培养的人体造血干细胞移植给小鼠后,可以保持造血能力。
由于添加到培养液中的细胞因子等蛋白质比化合物更昂贵,而且质量参差不齐。因此不用蛋白质有望实现价格便宜且稳定的培养。然而,与小鼠体内的增殖效率相比,体外培养造血干细胞尚未达到“飞跃性增加”(山崎教授)。今后研究团队将通过改进化合物的组合,实现更高效的培养。
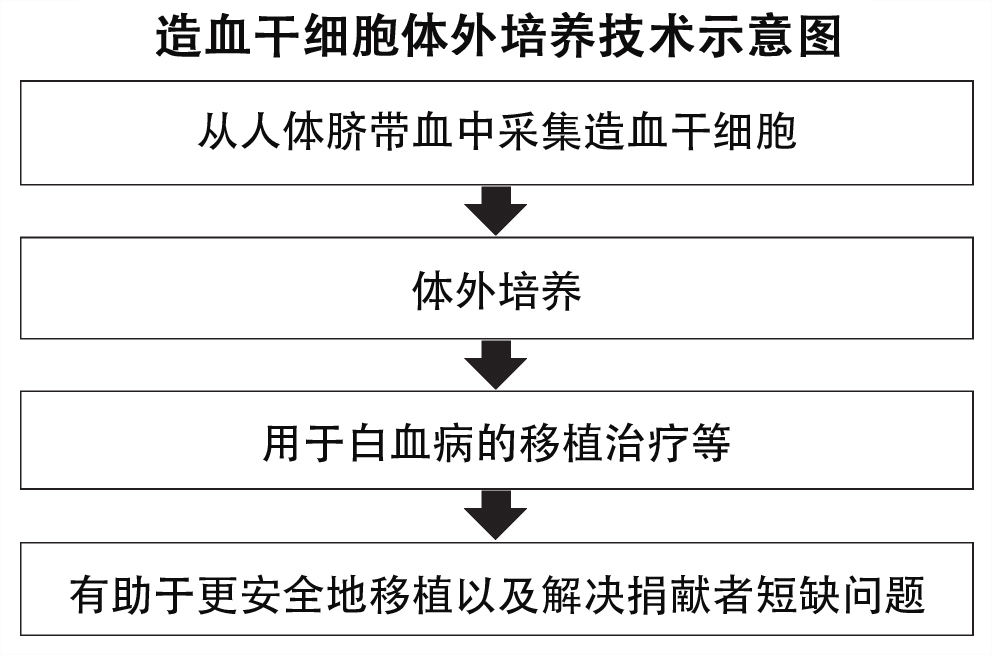
造血干细胞移植是治疗血液疾病的重要手段。对于无法用抗癌药物治愈的白血病、恶性淋巴瘤等难治性血液癌,以及无法正常造血的再生障碍性贫血患者,需要移植来自健康捐赠者的造血干细胞。
在造血干细胞移植方法中,骨髓移植在收集细胞时会给捐献者造成较大的生理负担。另一方面,脐带血中所含的造血干细胞数量又较少,移植后需要很长时间才能造血,增加了感染风险。如果能在体外增殖造血干细胞,既可以提高移植的安全性,又有助于解决捐献者短缺问题。
对于镰状细胞病等遗传性血液疾病,全世界正在研究基因疗法,即设法修复患者自身造血干细胞中的遗传因子异常后,将其返回体内。樱井专任讲师表示,造血干细胞培养技术“未来有望应用于基因治疗”。
原文:越川智瑛、《日经产业新闻》、2023/4/3
翻译:JST客观日本编辑部













