世界首个针对引起呼吸道疾病的RS病毒 (RSV) 的疫苗预计将于2023年率先在美国投入使用。婴幼儿和老年人感染RS病毒后,很容易引发肺炎等重症。尽管国内外制药巨头都在竞相研发疫苗,但最终或将还是欧美公司抢先抵达终点。
RS病毒会导致婴幼儿和老年人罹患肺炎等(供图:美国CDC)
2023年2月,在英国医学杂志《新英格兰医学杂志》上发表了英国葛兰素史克公司(GSK)研发的RS病毒疫苗国际联合3期临床试验结果。试验为60岁及以上的老年人进行单次疫苗接种后,调查了疫苗对下呼吸道感染的预防效果。实验分别为约12,000人接种疫苗和安慰剂,经过约半年时间的跟踪观察,疫苗组有7人出现症状,安慰剂组有40人出现症状。发病预防效果为82.6%,重症预防效果为94.1%。
GSK公司的疫苗使用对病毒表面的“F蛋白”进行基因改造后的蛋白质。2022年10月,在日本申请了以60岁及以上人群为对象的生产和销售许可。随后分别于10月末向欧洲药品管理局(EMA),11月向美国当局提出了申请。
美国预计将于2023年5月3日前公布审批结果。3月,美国食品药品监督管理局(FDA)咨询委员会认可了其疗效和安全性,在批准方面取得了重大进展。如果获批,将成为全球首个RS病毒疫苗。
RS病毒即一种引起普通感冒的病毒。即使成年人受到感染,通常症状也较轻。该病毒非常常见,据不完全统计,儿童在出生一年内有一半以上,两年以内接近100%会受到感染。
首次感染时,大约70%的感染者仅会出现流鼻涕等轻微症状,但约30%的感染者会因咳嗽加重而出现喘鸣等症状。出生未满半年的婴儿及患有基础心肺疾病的儿童一旦感染,较容易出现呼吸困难等严重症状。老年人也存在引发肺炎最终导致死亡的情况发生。目前虽然已有针对婴幼儿的抗病毒药物,但疫苗尚未面世。
美国辉瑞公司正致力于研制针对孕妇和老年人的RSV疫苗。针对孕妇的疫苗方面,公司于2022年11月公布了中期分析结果,确认了国际联合3期临床试验的有效性和安全性。结果显示,产后未满90天的婴儿中,由RS病毒引发的严重下呼吸道疾病的入院比例减少了81.8%。未满6个月的婴儿的入院比例也下降了69.4%。
从数据来看,产后未满90天婴儿的发病预防效果为57.1%,产后未满6个月婴儿的发病预防效果为51.3%,该数值未达到预期的成功标准。东京医科大学准教授柴田岳彦解释说:“由于从母体获得的移行抗体(出生后日渐)减少,效果自然会降低。”辉瑞公司已于2023年2月在日本提交审批申请。
2022年8月,一项针对老年人的疫苗临床试验结果公布显示预防重症的有效率为87.5%。12月,其向美国当局申请审批并获得优先审查资格。审批结果预计将于2023年5月宣布。
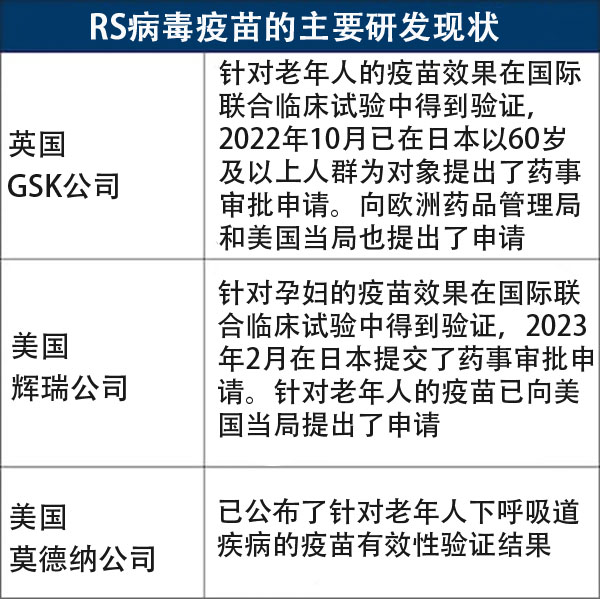
2023年1月,美国莫德纳公司宣布使用信使RNA(mRNA)的针对老年人的RS病毒疫苗对下呼吸道疾病的有效性为83.7%。据非营利组织PATH称,截至2023年1月,美国杨森制药公司正在进行三期临床试验,日本第一三共公司和法国赛诺菲公司也在进行二期临床试验。
RS病毒疫苗的研发历史非常悠久。在1960年代,为婴幼儿接种尚处于研发中的疫苗后,由于病毒感染症状加剧还出现过死亡病例。
研发迟迟无法进展的原因是病毒蛋白质的形状难以作为疫苗制造。虽然RS病毒表面的F蛋白质在与细胞膜融合之前更容易产生效果,但由于形状不稳定,即使制成蛋白质,也会变成融合后的形状。
转折点出现在2013年。美国国立卫生研究院 (NIH) 发现,即使在融合之前,也可以通过突变蛋白质的一部分来稳定蛋白质的形状。在此基础之上,才有了目前多种处于临床试验阶段的疫苗。
日文:藤井宽子、《日经产业新闻》、2023/3/29
中文:JST客观日本编辑部













