通过更易于使用的低分子药,达到与使用了RNA(核糖核酸)等的“核酸医药”同等效果的研究正在推进之中。美国斯克利普斯研究所开发的名为“RIBOTAC(核糖核酸酶靶向嵌合体)”的技术,就是利用低分子来分解疾病根源RNA的,动物实验确认了其对癌症和ALS(肌萎缩性侧索硬化症)的效果。2名日本人为该技术的开发做出了贡献,日本国内企业也开始探讨该技术。

开发成功RIBOTAC的美国斯克利普斯研究所的马修·迪斯尼教授(左)和田边三菱制药的松本安正主任研究员(提供:田边三菱制药)
核酸医药近年来应用越来越多,为遗传性疑难病症等的治疗带来了新机遇。核酸医药的原理是作用于从DNA复制遗传信息RNA,并抑制目标基因的影响。治疗中使用的人工核酸优势在于,易于根据病症设计,可以在短时间内合成新药候补。但由于分子较大,要将其输送到患部,需要花费一番努力,同时可作为对象的脏器也有很多制约。
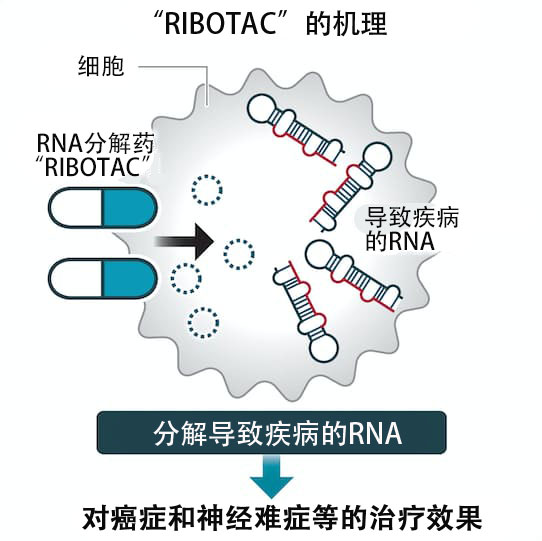
RIBOTAC是比核酸更容易作为药剂使用的低分子药,同时可以发挥与核酸医药同等的作用。其原理是,在细胞内分别与分解RNA的酶及致病的RNA相结合,使二者接近并促使其分解。与核酸药物相比,RIBOTAC的设计难度更大,但理论上可以输送到所有器官,不仅可以用作点滴药,也可以制成口服药。这是斯克利普斯研究所教授马修·迪斯尼等人于2018年发表的技术。
“RIBOTAC能克服核酸医药的缺点”。参与开发的田边三菱制药的松本安正主任研究员也为这项技术做出了贡献。
松本安正主任研究员感受到了作用于蛋白质的传统药物的局限性,并于2016年到2018年到RNA研究第一人的迪斯尼教授身边留学。他成功合成了分解与癌症增殖相关的MicroRNA这种低分子,并在有效治疗药物较少的乳腺癌细胞上确认了效果。
研究的出发点,是作为分解蛋白质的治疗药进行开发的“PROTAC(蛋白降解靶向联合体)”。二者都是利用了细胞所具备的分解机制的低分子药,而问题是如何将分别与MicroRNA及RNA分解酶结合的分子连结起来。化学合成专业的松本主任研究员花了大约半年的时间成功解决了这一问题。
另一位从2018年到2021年在迪斯尼教授身边学习的是东京大学的相川春夫助教。他将与RNA分解酶相结合的分子小型化,使其更易于在生物体内发挥作用,并在小鼠实验中抑制了癌症向肺部的转移。
相川助教等人证实了这项技术应用于肌肉逐渐僵化的疑难病症ALS上的可能性。ALS被认为是由特定基因的RNA中发现的碱基反复序列引起的。一般的反复在20次左右,而超过100次就会引发病症,在RNA中形成发夹状结构,在细胞内结块,从而使神经细胞受损。研究人员通过合成与该结构结合并分解RNA的化合物,成功减少了小鼠细胞内的结块。
RIBOTAC与核酸医药相比,还有减少副作用的可能性。在ALS中发现的碱基反复序列中,长度较短的序列也存在于另一个基因的RNA中。核酸药物也会作用于这样的RNA,而RIBOTAC只会分解使ALS发病的RNA。核酸药物作用于碱基序列,而RIBOTAC作用于RNA结构。RIBOTAC“能超越核酸医药的界限”(相川助教)正是因为它的这个特征。
日本国内企业也开始了相关开发。RNA制药公司veritasinsilico(VIS、东京・品川区)于2022年宣布,将与对药品开发提供支持的Axcelead Drug Discovery Partners(ADDP,神奈川县藤泽市)共同开发探索RIBOTAC化合物的技术。VIS的中村慎吾社长表示:“希望能够开发出效果更好的化合物。”
用于RIBOTAC的化合物等“要素”正逐步齐全。虽然这还是一项处于黎明时期的技术,但它隐含着能极大程度改变药品开发方式的可能性。
日文:远藤智之、《日经产业新闻》、2023/2/8
中文:JST客观日本编辑部













