新一代癌症治疗药物“靶向蛋白降解药”的研发势头正盛。因能针对性攻击引起疾病的蛋白质(病原蛋白)有望获得较高疗效而颇受期待。安斯泰来制药表示将正式投入经营资源,率先在日本企业中首次开展临床试验。引领该公司研发的是蛋白降解药部门长早川昌彦。

安斯泰来制药蛋白降解药部门长早川昌彦
——靶向蛋白降解药是一种怎样的药物?
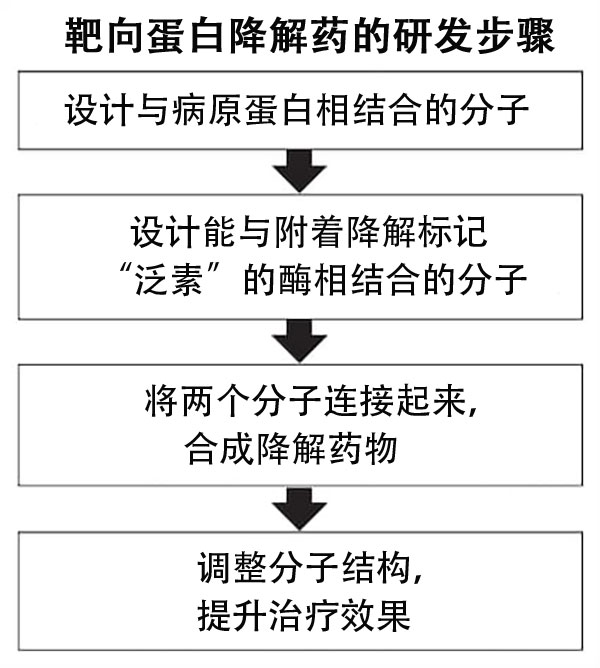
早川:是一种促进病原蛋白分解的低分子药物(低分子化合物类药物)。它利用了细胞原本就具备的能够分解非需要蛋白质的机制。让作为分解标记的泛素分子与病原蛋白、以及附着在病原蛋白上的酶相结合,就可以将两者联在一起促进分解。
以往的癌症治疗药物主要是抑制剂型,它与癌细胞增殖相关的蛋白质相结合以阻碍其功能。然而,能与治疗药物紧密结合的“深口袋”病原蛋白仅约两成左右,对于除此之外的癌细胞则难以开发治疗药物。降解药物即便口袋很浅也能发挥作用,理论上可以把所有病原蛋白作为攻击目标。
——2022年美国已开始了临床试验。
早川:临床试验的对象是特定基因变异导致的大肠癌。这种基因变异引发的肿瘤中,名为KRAS蛋白质的第12个氨基酸从甘氨酸替换成了天冬酰胺。由于结合口袋浅,治疗药物开发较为困难。能进入临床试验正好是因为降解药物才得以实现的成果,希望最早在2023年内就能得出结果。
——药物开发有可能发生怎样的改变?
早川:这关系到一些已放弃研发药物的重生。美国临床试验中的候选新药,将作为抑制剂效果不佳的药物改为降解药物的“零件”,使其重生。换句话说就是把过去的失败变成了宝库。
此外靶向蛋白降解还有利于提高药物开发效率。通常药物的合成需要几年时间,但此次降解药物的合成仅用了5个月,这一速度是空前的。此前也有合成数千种以上药物的情况,但此次在合成第38种药物时就得到了能够进入临床试验的候选药物。除了对可用于降解药物使的各种成分(分子)进行高效搜索外,药物设计还使用了人工智能(AI)和机器人技术。
——对安全性等方面有顾虑吗?
早川:我认为可以开发出仅对体内的针对性部位起作用的降解药物。可在病原蛋白上附着泛素的酶约有600种,有的会在特定的癌部和器官中发挥作用。所以可以根据药物设计的不同来使用适当的酶。
目前针对其它病原蛋白的降解药物也在开发中。希望将来也能应用于免疫疾病等。虽然有人说(经过多年推进的)低分子药物的研发已经到了极限,但降解药物的出现让人们切实感受到低分子药物还大有可为。
利用研究的积累来改变落后局面
国外的企业在开发靶向蛋白降解药方面处于领先地位。美国初创企业Arvinas正与美国大型制药公司辉瑞共同以乳腺癌患者为对象开展临床试验。2022年宣布其研发的药物在第二阶段临床试验中对38%的患者有效,最快2023年内将开始最终阶段的临床试验。
虽然目前还没有成功将靶向降解药物用于实际治疗的案例,但近年来的研究表明,用于治疗多发性骨髓瘤的沙利度胺类抗癌药的作用机制与降解药物相同。沙利度胺类药物的年销售额超过1万亿日元,期待靶向降解药物中也能出现优秀的癌症治疗药物。
日本从早期开始就为降解药物的研发和机制阐明做出了贡献。早川表示“日本有很多低分子药物所需的化学合成专家”,如果能发挥这一优势,日本还有充分的机会改变局面。
日文:远藤智之、《日经产业新闻》、2023/1/30
中文:JST客观日本编辑部













