山梨大学研究生院综合研究部医学域药理学讲座教授小泉修一、副教授筱崎阳一的研究团队,发现了与原因不明的正常眼压性青光眼发病有关的分子。
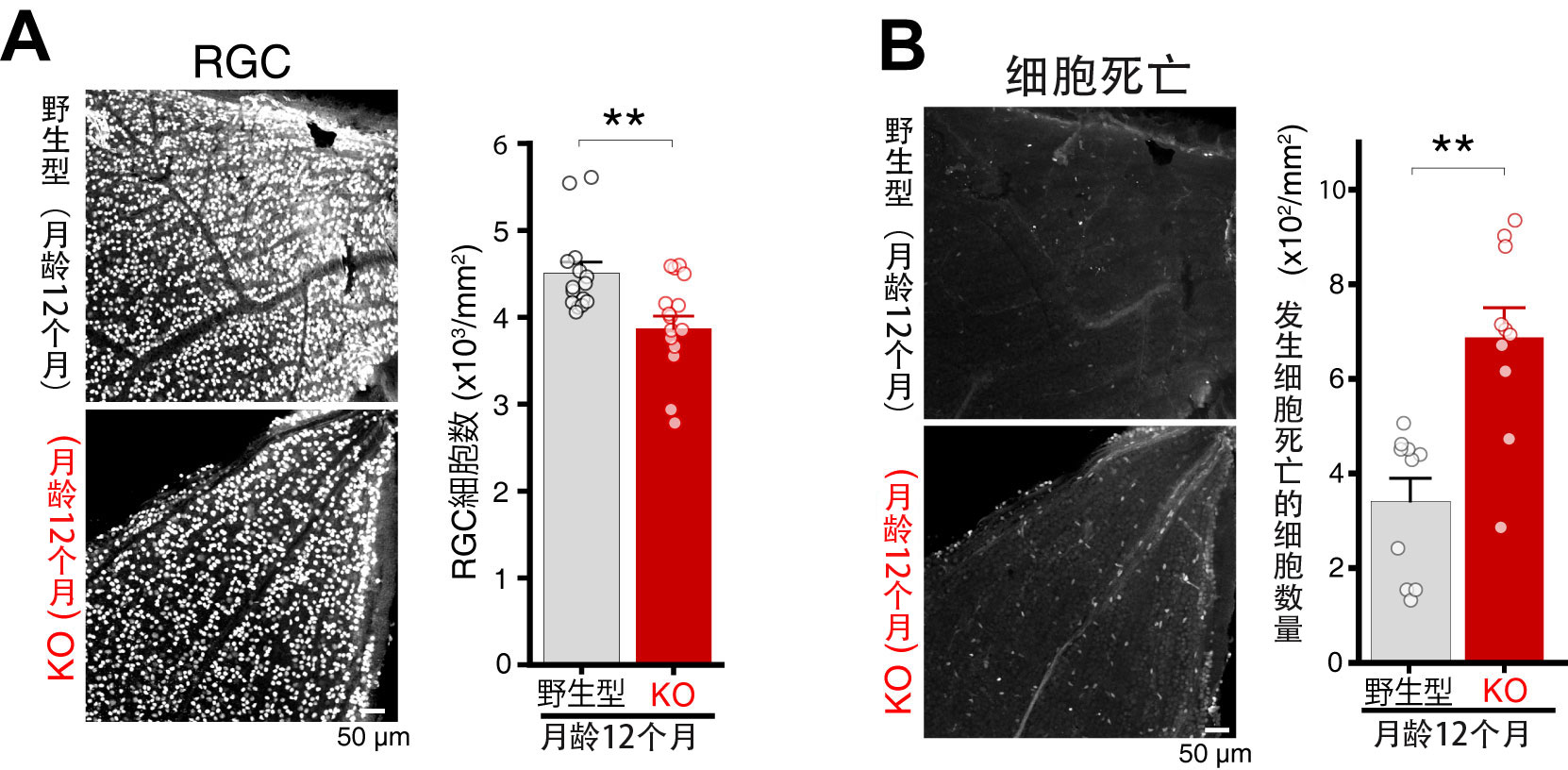
图1 ABCA1KO小鼠的RGC脱落和细胞死亡
(A)测量12个月月龄小鼠视网膜的RGC数,发现与野生型小鼠相比,ABCA1KO小鼠的RGC数显著减少(**表示显著性差异)。(B)另一方面,用染色检测出细胞死亡进行评估,发现ABCA1KO中引起细胞死亡的细胞数量显著性增加。(供图:山梨大学)
青光眼是日本导致中途失明的头号疾病。高眼压是最大的风险因素,但日本患者中的大部分为正常眼压性青光眼,查明眼压以外的病因是当务之急。最近,多个全基因组关联分析报告显示,“ABCA1”基因变异与青光眼有关,但至今仍不清楚为何ABCA1变异会导致青光眼发病。
研究团队在全球青光眼患者基因变异分析数据库(GWAS)中发现了ABCA1异常的现象,并进行了分析。研究团队首先探讨的是与青光眼发病有关的原因是ABCA1功能的缺失还是异常功能的获得。研究团队使用全身缺失ABCA1的小鼠,调查了其对视网膜神经节细胞(RGC)的影响。结果发现,与正常小鼠(野生型小鼠)相比,基因缺失小鼠在12个月月龄时视网膜的RGC数显著减少。
接下来,研究团队使用了多种方法评估ABCA1在哪个细胞中表达,结果发现ABCA1在分布于视网膜最内层及视神经的一种非神经细胞胶质细胞——星形胶质细胞中表达最为丰富。因此,研究团队制备并评估了星形胶质细胞表达缺失的小鼠。与12个月月龄的对照小鼠(Ctr)相比,缺失小鼠的RGC数显著减少,死亡细胞数量增加。
为了明确分子机制,研究团队进一步通过单细胞RNA测序进行了分析,发现被称为趋化因子的分子在RGC和星形胶质细胞中发生相同的变化。对RGC的详细分析表明,特定的细胞群特别容易受到伤害。此外,离子通道型谷氨酸受体子单元之一Grin3a(编码谷氨酸受体亚型NR3A的基因)的表达因ABCA1缺失而大幅减少。由于NR3A会抑制谷氨酸引起的神经兴奋,所以可认为NR3A表达降低会导致过度的神经兴奋和兴奋性毒性引起的神经细胞死亡。
该研究成果源于与伦敦大学(UCL)眼科学研究所Alex Leung研究生、大沼信一教授开展的国际共同研究,并在东京都医学综合研究所原田高幸参事研究员、生理学研究所超微形态研究部门及自治医科大学解剖学讲座大野伸彦教授、新泻大学研究生院医齿学综合研究科脑功能形态学领域竹林浩秀教授、山梨大学研究生院综合研究部眼科学讲座柏木贤治教授、该大学综合分析实验中心濑川高弘讲师、社会医学讲座三宅邦夫副教授等人的协助下完成。
小泉教授表示:“星形胶质细胞和青光眼一直没能联系起来,此次我们发现ABCA1缺失会导致视网膜星形胶质细胞发炎,从而引发青光眼症状。今后,我们希望评估抑制星形胶质细胞异常的候选化合物的视神经保护效果,探索新的正常眼压性青光眼的治疗药物。”
【词注】
■星形胶质细胞是一种胶质细胞,属于最大、数量最多的细胞种类,一直被认为负责脑内的支持和恒常性的维持。最近研究表明,星形胶质细胞也积极地参与大脑的信息处理。它也存在于视网膜的最内层表面和视神经周围。
原文:《科学新闻》
翻译编辑:JST客观日本编辑部
【论文信息】
杂志:Science Advances
论文:Astrocytic dysfunction induced by ABCA1 deficiency causes optic neuropathy
DOI:10.1126/sciadv.abq1081













