北海道大学研究生院医学研究院肿瘤病理学教室及该校创成研究机构化学反应创成研究基地(WPI-ICReDD)的田中伸哉教授和津田真寿美副教授等人组成的研究团队,全球首次成功地利用从大肠癌患者体内切除的癌组织切片上评估了每位患者的癌细胞有多大的移动能力。
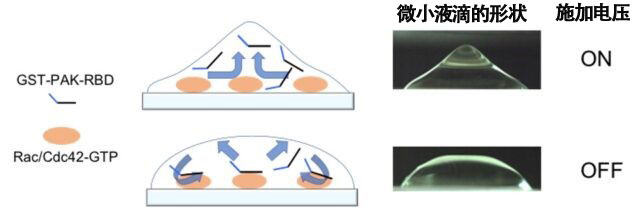
利用电场非接触搅拌技术改变微小液滴的形状。通过反复施加低频电压并高速搅拌含GST-PAK-RBD探针的液体,成功地使GST-PAK-RBD探针快速与癌细胞内被激活的Rac/Cdc42(Rac/Cdc42-GTP)特异性结合。(提供:北海道大学)
癌细胞的移动能力(运动和浸润能力)由低分子量G蛋白Rac和Cdc42控制,这些分子越活跃,癌细胞的移动能力越强,越容易向血管和淋巴管中侵袭和转移。此前一直通过Rac/Cdc42拉下实验对癌细胞的运动和浸润能力进行生化评估。但这样会完全失去在癌组织内的位置信息,也无法评估细胞的异质性。
为此,研究团队利用近年来开发的电场非接触搅拌技术,在用于病理诊断的癌组织切片上(FFPE样本)以极高的速度搅拌与被激活的Rac/Cdc42相结合的探针溶液,能够快速并特定性评估大肠癌细胞的运动和浸润能力。
评估结果显示,细胞的Rac/Cdc42活性①与大肠的正常粘膜相比在肿瘤区域显著升高;②癌细胞的恶化阶段越高,Rac/Cdc42的活性越高;③在癌细胞浸润周围正常组织的尖端尤其高。另外还发现,④Rac1/Cdc42活性较高的病例容易发生淋巴管浸润。
津田副教授表示:“在该技术开发过程中,我们为如何抑制染色背景和检测特异性信号而苦恼。这项技术不仅适用于大肠癌,还适用于乳腺癌和脑肿瘤,并有望在预测癌细胞的淋巴结转移,以及未来将Rac抑制剂用于伴随诊断时提供重要信息。”
【词注】
Rac/Cdc42:低分子量G蛋白Rho家族的主要成员。在GTP(鸟苷三磷酸)与Rac和Cdc42结合时激活,GDP(鸟苷二磷酸)与Rac和Cdc42结合时失活。被激活的Rac/Cdc42会促进癌细胞的运动和浸润能力。
原文:《科学新闻》
翻译编辑:JST客观日本编辑部













