核心要点:
1. 免疫检查点蛋白PD-L1是免疫治疗的重要靶点,癌症组织中PD-L1的表达量与免疫治疗的效果显示临床相关性。
2. 本研究开发了一种新型的D型多肽核药,该药物可以特异性检测肿瘤组织中的PD-L1的表达量,从而为免疫治疗提供指导。
3. 该核药通过释放β射线,可以选择性杀死肿瘤组织中的PD-L1高表达的癌细胞,是一种潜在的癌症治疗药物。
4. 该研究表明D型多肽是理想的靶向核素递送分子,为多肽核药开发提供了新的研究方向。
国立研究开发法人量子科学技术研究开发机构量子生命・医学部门量子医科学研究所先进核医学基础研究部胡宽研究员,张明荣部长等人开发了一种新型的多肽核药用于癌细胞中PD-L1的显像,并证明了该核药具有一定的肿瘤治疗效果。该成果于近日发表在重要的药学期刊《Acta Pharmaceutica Sinica B》。该研究的合作者包括来自中国南京市第一医院、北京大学深圳研究生院以及深圳湾实验室的研究人员。
研究背景
近年来,免疫治疗成为了继化学治疗、放射性治疗、靶向治疗后,最重要的癌症治疗手段之一。过去五年,基于免疫检查点抑制剂的免疫治疗取得了巨大的成功。目前,多种针对免疫检查点蛋白PD-1/PD-L1/CTLA-4的单克隆抗体药物已经进入市场,为患者提供了更多的治疗选择。但是,免疫检查点治疗也表现出一些不足。比如:只有部分病人对免疫检查点治疗显示临床受益。因此,如何筛选出潜在的受益人群,从而避免无效治疗,是仍旧存在的医学难题。
基于临床数据分析,研究人员发现肿瘤组织中PD-L1的表达量与免疫检查点治疗效果呈现密切的相关性:高表达PD-L1蛋白的病人在接受免疫检查点抑制剂治疗后,表现出更佳的临床受益。因此,非侵入性检测肿瘤组织中的PD-L1表达量,可以筛选出适合免疫检查点治疗的病人,从而提高治疗的有效性和准确性。
截至目前,来自美国、中国等国家的科学家相继开发了可以特异性显像PD-L1的核医学诊断试剂。日前,多个诊断药物已经在美、中分别进入临床试验阶段。与美、中相比,日本尚未有免疫检查点显像药物进入临床。尽管本庶佑教授因为对免疫治疗领域的巨大贡献获得了诺贝尔奖,但是,日本在免疫检查点显像药物的开发方面投入明显不够。
日本国立量研机构张明荣教授团队于2018年开始启动了免疫检查点显像药物的开发项目,在过去三年,相继发表了多篇重要论文,公开了该团队在免疫检查点显像药物开发方面的系列进展。该团队从药物分子创制出发,旨在开发出可以用于临床的免疫检查点显像药物。
研究内容
在该研究中,研究者将目光投向了一类新型的多肽分子—D型多肽。D型多肽是一类全部由D型氨基酸组成的多肽。D型多肽的研究始于上个世纪70年代,经过接近半个世纪的发展,人们对于D型多肽的结构、活性、活体代谢情况有了深刻的认识。D型多肽不仅保留了L型多肽的优点,如:优良的药代动力学性质、优异的靶点特异性以及低毒性。而且,与L型多肽不同,D型多肽难以被天然的水解酶识别降解,从而在活体内具有极强的稳定性。研究表明D型多肽较L型多肽具有更长的胃肠道、血浆以及细胞内的半寿命。此外,一些包含有D型氨基酸的多肽已被批准用于临床,如Vasopressin,Desmopressin,DOTATATE等,这些结果表明D型多肽具有良好的生物安全性。鉴于以上优点,研究人员推断D型多肽是潜在的核素显像药物的靶向载体。
研究者选择了一条由十二个氨基酸组成的D多肽—DPA作为研究对象。DPA由噬菌体展示筛选得到,其具有特异性结合PD-L1的能力。作者首先研究了DPA在活体小鼠内的分布、吸收和代谢情况。研究者使用正电子核素64Cu对DPA进行了标记,接下来在正常C57BL/6J老鼠体内追踪了[64Cu]DPA的运动情况。结果表明,[64Cu]DPA被快速的从血浆中清除,并主要经由肾脏排出体内(图1)。通过尿液分析表明,[64Cu]DPA在体内未发生降解,直接以完整的分子形态从尿液排出。
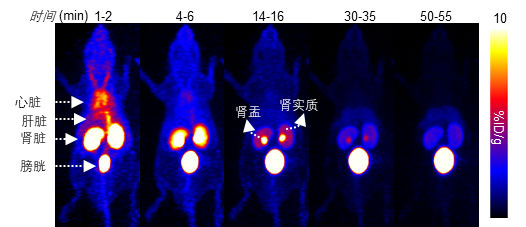
图1. [64Cu]DPA在小鼠体内随着时间的分布变化动态图。
随后,研究人员分别在荷有B16F10和U87MG肿瘤的小鼠中进行了[64Cu]DPA成像,结果显示,在尾静脉注射后的80分钟以内,[64Cu]DPA在瘤内有明显的富集,这些结果表明[64Cu]DPA在活体内可以有效的结合PD-L1,从而进行PD-L1表达量的检测。但是,考虑到64Cu的物理半衰期为12.7h,与DPA的靶点作用时间不匹配,随后研究人员使用68Ga对DPA进行了标记。68Ga是一种短寿命的正电子发射核素,其半衰期为68min。在荷U87MG肿瘤的小鼠体内的显像结果表明[68Ga]DPA是一种具有临床转化潜力的PD-L1的显像分子(图2)。
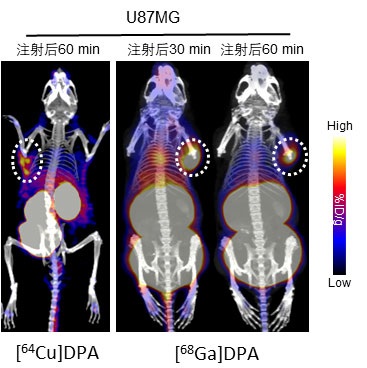
图2. [64Cu]DPA和[68Ga]DPA在U87MG异种移植小鼠中的分布图。
最后研究人员进一步研究了[64Cu]DPA作为一种靶向PD-L1的核素治疗分子对U87MG肿瘤生长的抑制情况。由于64Cu可以发射β负电子以及俄歇电子,单次尾静脉注射74MBq的[64Cu]DPA,即显示出对U87MG肿瘤的生长抑制效果(图3)。此外,[64Cu]DPA也表现出良好的生物安全性,在治疗期间,除了由于放射性引起的白细胞先减少后增多现象,未观察到其他明显的毒副作用。这些结果表明[64Cu]DPA是一种潜在的靶向核素治疗药物分子。
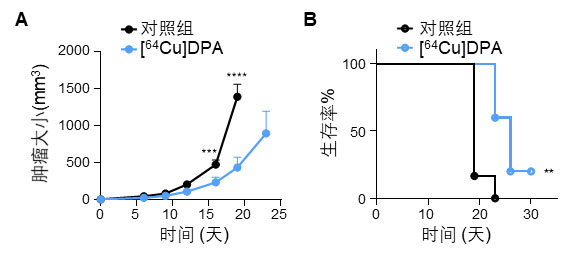
图3. 肿瘤变化曲线(A)和小鼠生存曲线(B)。
研究结论
该论文开发了一种新型的PD-L1的诊断核药物,该药物由特异性识别PD-L1的D型多肽和正电子核素组成。在黑色素瘤和脑胶质瘤模型中,该药物成功对PD-L1的表达进行了检测。此外,当与64Cu结合时,该药物还显示出一定的治疗效果。未来,通过对该药物的进一步优化,有可能得到一种可临床转化的集诊断和治疗功能一体的新型核药。
论文信息:
论文题目: Whole-body PET tracking of a D-dodecapeptide and its radiotheranostic potential for PD-L1 overexpressing tumors
刊载期刊 Acta Pharmaceutica Sinica B
论文链接:doi.org/10.1016/j.apsb.2021.09.016
文 胡宽
编辑修改 JST客观日本













