东京医科齿科大学研究生院医齿学综合研究科的横田隆德教授和永田哲也副教授通过与爱奥尼斯制药公司和武田药品工业公司开展联合研究,开发出了突破常规核酸药物无法有效通过的血脑屏障,可通过静脉注射和皮下注射抑制中枢神经系统的基因表达的血脑屏障(BBB)通过型异源双链核酸。虽然脊髓性肌萎缩症的核酸药物已经获批,难治性神经系统疾病的根治正逐渐变为可能,但由于必须终生持续向鞘内注射药物,患者的负担非常大,而此次开发的技术,患者可以自己进行皮下注射。横田教授表示:“(该药物)应用于已批准的几种异源核酸药物后确认,具有5倍至100倍(平均20倍左右)的超强基因抑制效果。另外,还考虑将该药物应用于阿尔茨海默病等,目前正与多家制药公司进行联合研究”。相关成果已经发布在《Nature Biotechnology》上。
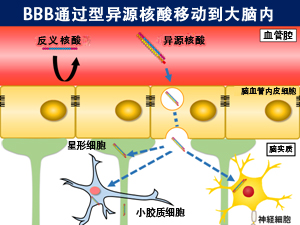
血脑屏障通过型异源核酸会穿过脑血管内皮,移动到大脑内,被神经细胞、小胶质细胞和星形胶质细胞吸收,发挥抑制基因表达的效果。而单链反义核酸不会穿过脑血管内皮。(图片由东京医科齿科大学提供)
核酸药物是一种先进生物医药技术,可以选择性控制以往的低分子化合物和抗体药物难以控制的靶标RNA。近3年来,脊髓性肌萎缩症、家族性淀粉样多发性神经病及杜氏肌营养不良症等神经和肌肉疾病领域已经有15种核酸药物通过审批。另外,肌萎缩侧索硬化症、帕金森症和阿尔茨海默病等多种中枢神经系统疾病也在进行临床试验。
但是,治疗中枢神经系统疾病时,需要进行腰椎穿刺直接向鞘内注射药物。因为以往的反义核酸和siRNA等核酸药物全身给药时无法通过血脑屏障,药物无法到达大脑和脊髓等中枢神经。
鞘内给药是从后背的腰椎缝隙将一根长针插入脊髓周围的脊液中给药的方法,老年人中常见的接受抗凝治疗的患者,以及难治性神经系统疾病中常见的脊柱侧弯患者则很难通过这种方法给药,偶尔也会发生感染和出血等。
东京医科齿科大学的联合研究团队虽然已经独立开发出了拥有与常规核酸药物不同的分子结构和多样化的递送分子,以及凭借独特的细胞内作用机制而高度有效的DNA/RNA异源双链核酸,但大脑的控制则比较难。因此,研究团队尝试使各种脂质传递分子(配体)与互补链结合,筛选了血脑屏障通过性药物。由此发现,结合胆固醇注射到小鼠的静脉中时,显著抑制了中枢神经系统中的靶标RNA。这种效果通过多次给药得以加强。
另一方面,以往的单链反义核酸无论单次给药还是多次给药都未能发现抑制中枢神经系统基因表达的效果。此外,研究团队还利用在单链反义核酸中直接结合胆固醇的核酸进行了比较,确认这种方法效果较弱,且具有高毒性。
研究团队利用新开发的血脑屏障通过型异源双链核酸进行静脉注射后确认,药物被递送到中枢神经系统中,并抑制了各种靶标RNA在中枢神经系统中的基因表达。详细调查在神经细胞和各种胶质细胞中的基因表达的抑制效果后发现,在神经细胞和小胶质细胞中发现了强烈的基因表达抑制效果。共聚焦激光显微镜的实时图像显示,只有血脑屏障通过型异源双链核酸明显移动到了大脑中。
除静脉注射外,皮下注射也观察到了中枢神经系统的基因表达抑制效果,这样患者就无需每次都去医疗机构,可以自己进行皮下注射,存在大幅提高患者便利性的可能。
原文:《科学新闻》
翻译编辑:JST客观日本编辑部













