日本横滨市立大学学术院医学群的宫城悦子教授、平野久名誉教授,和该校先端医科学研究中心的荒川宪昭客座副教授(兼任日本国立医药品食品卫生研究所主任研究官)的研究团队,与东曹公司(代表董事社长:山本寿宣)于7月28日宣布共同研发出了卵巢透明细胞癌的新型诊断标志物。通过蛋白质组分分析发现,卵巢透明细胞癌会特征性产生“TFPI2(组织因子途径抑制物2)”,并以此与东曹共进行了同研发,以期通过“TFPI2”与现有的卵巢癌标志物的联合检查,进一步为今后的诊断和治疗提供有效参考。相关论文已发表于国际科学期刊《International Journal of Clinical Oncology》。
(图片由横滨市立大学提供)
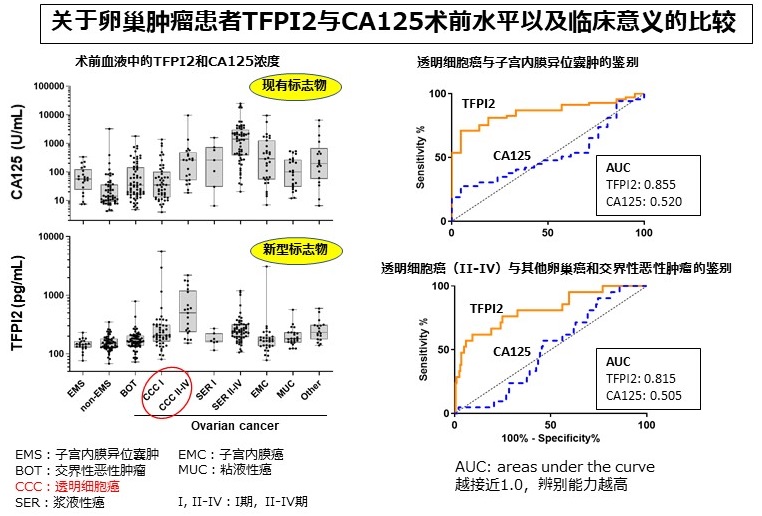
日本每年大约有1万人被诊断为上皮性卵巢癌,其中约4500人死亡。该病分为4种组织学类型,即浆液性癌、透明细胞癌、子宫内膜癌和粘液性癌,其中透明细胞癌占具25%。
透明细胞癌由良性肿瘤子宫内膜异位症发展而来,在年轻人中呈增加趋势,且产生化疗耐药性而预后不良的病例较多。同时,现有的卵巢癌标志物检出结果偏低或出现伪阴性的病例也相对较多。虽然,现有的卵巢癌标志物CA125能以高灵敏度检测出所有类型的卵巢癌,但对于特定的透明细胞癌而言,目前难以通过与其他标志物的联合诊断予以区分,因此需要开发能高精度检测透明细胞癌的新型生物标志物。
横滨市立大学在日本文部科学省“创新系统整备事业”项目的支援下,设立了拥有十多台质谱仪的分析中心。
研究之初本考虑通过这些质谱仪全面分析患者的血液等样本,以此来寻找源自透明细胞癌的蛋白质。然而在血液中,主要源自肝脏的球蛋白等蛋白质的含量是源自癌症的蛋白质含量的约10亿倍,因此难以测得。
为此,研究团队着眼于妇产科研究室保有的大量癌细胞培养株。在通过质谱仪对透明细胞癌、粘液性癌和浆液性癌的癌细胞培养株的培养液进行蛋白质组分分析后,确定了891个源自透明细胞癌、1085个源自粘液性癌、和948个源自浆液性癌的蛋白质。然后从中发现了148个仅来自于透明细胞癌的蛋白质,其中之一就是被确立为新的卵巢癌标志物的“TFPI2”。
“TFPI2”是宫城教授等人于1993年在探索癌细胞分泌的生物活性物质过程中发现的胎盘特异性表达的蛋白酶抑制蛋白。
为了将“TFPI2”作为新型卵巢癌标志物使用,研究团队与东曹公司共同开发了利用两种抗体检测血清中此蛋白的检测试剂。利用这种试剂和全自动酶免疫分析仪,可在20分钟内能完成检测。
为验证该检测试剂的性能,研究团队在横滨市立大学和奈良县立医科大学针对对包括透明细胞癌在内的425名妇科患者进行了血清中“TFPI2”浓度的测定,并与现有标志物CA125的性能进行了比较。
通过验证实了“TFPI2”以高浓度特异性存在于透明细胞癌患者的血液中。并表现出不同于现有标志物的特征,提示其有成为新诊断标志物的可能性。
之后,研究团队继续在日本的五家医疗机构(横滨市立大学、奈良县立医科大学、神奈川县立癌症中心、兵库县立癌症中心、静冈县立癌症中心)进行了旨在以实用化为目标的临床性能试验。通过测量需要接受手术治疗的351例卵巢肿瘤患者术前血清中“TFPI2”的水平,确认了此蛋白质在透明细胞癌中特异性升高。在274例卵巢恶性肿瘤患者中,“TFPI2”检测透明细胞癌的特异性高达80%,由此其实用性得到了证明。另外本实验中还证实了, “TFPI2”和CA125的联合检测,能大幅提高1期(初期)透明细胞癌的检测灵敏度。
基于这些结果,“TFPI2”作为体外诊断药物获得了日本的制造销售许可,已于今年4月被纳入医保范围,并7月下旬开始投放于临床应用。
卵巢透明细胞癌在亚洲人中相对常见,与其他妇科类疾病不同,抗癌药的效果并不明显。因此在临床实践中,有望利用“TFPI2”来辨别CA125呈阴性或低值的病例以及进行其与良性子宫内膜异位症的鉴别诊断,从而判断是否需要手术治疗等。
今后研究团队还将继续调查“TFPI2”在术后和使用抗癌药治疗前后的血中动态变化,以及良性子宫内膜囊肿的癌变过程,以期阐明其产生机制。 ..
对提高QOL和个性化医疗的期望
宫城教授表示:“对我们医生来说,‘TFPI2’能帮助医生制定医疗计划,以便在第一次手术中就尽量彻底切除卵巢透明细胞癌,‘TFPI2’的优点在于可以让我们为根治性手术提前做准备。当然,对患者来说,这也意味着能接受更好的治疗,旨在提高他们的QOL(生活质量),并有助于实现个性化医疗。”
原文:《科学新闻》
翻译编辑:JST客观日本编辑部













