大阪大学研究生院理学研究科博士后期课程的学生野村幸汰(日本学术振兴会特别研究员DC)与真木勇太助教、冈本亮讲师、梶原康宏教授及冈山大学健康系统综合科学研究科的佐藤Aya副教授等人组成的研究团队,通过以硫代酸为关键物质,开发出了完全不同于以往的糖蛋白合成方法,由此实现了在免疫过程中至关重要的细胞因子——糖链结合型C-C基序趋化因子配体1(CCL1)及白细胞介素3(IL3)的化学合成。另外,研究团队还通过细胞实验分析了造血细胞上的IL3受体与通过该合成法合成的IL3结合形成复合体时糖链所发挥的功能。由于可以将糖链自由嵌入蛋白质中,探究糖链在糖蛋白中功能的研究有望取得进展。此外,糖蛋白和糖肽制剂等高分子~中分子药品的合成效率也有望提高。相关研究成果已发布在《Journal of the American Chemical Society》上。
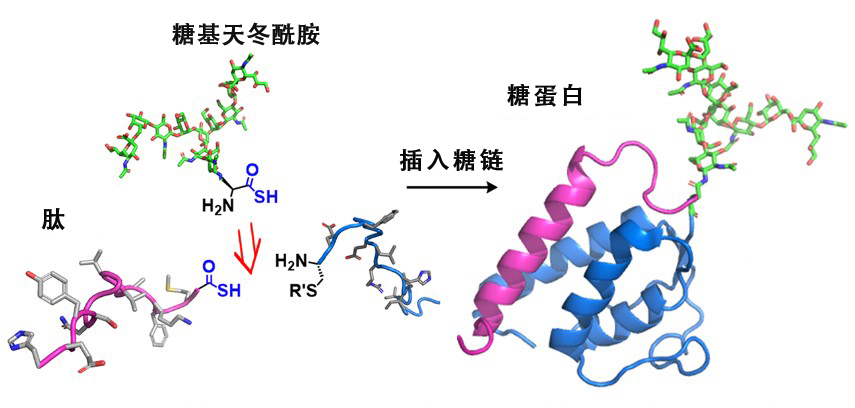
新的糖蛋白合成方法。通过以化学方法将糖基天冬酰胺嵌入到蛋白质中实现了糖蛋白的快速合成(图片:大阪大学提供)
糖蛋白具有对病毒产生免疫反应和炎症反应,以及向细胞传递信号等多种功能,但与体内的蛋白质结合的糖链有多种结构,很难确定哪种结构的糖链比较重要。另外,利用生物技术获得高纯度的糖蛋白也非常困难。
解决这个问题的对策之一是可以自由改变糖链结构,且能获得高纯度糖蛋白的化学合成法。但是以往的糖蛋白合成法平均需要100多个合成步骤,很难简单合成。
针对这些问题,上述研究团队为发展合成结构均一的糖蛋白的高效方法,很早就开始利用从鸡蛋中分离出来的糖链,研究拥有各种糖链结构的糖蛋白的化学合成。其中,在后期将糖链插入蛋白质分子的方法作为难度最大,效率最高的合成方法,一直在该团队考虑之中。然而,由于蛋白质和糖链存在各种各样的官能基,像低分子药物那样精确控制分子结构进行连接的方法在以前比较困难。因此需要开发精确控制蛋白质(肽)分子的化学选择性反应。
研究团队通过以硫代酸为关键物质,开发出了可通过化学选择性连接糖基天冬酰胺硫代酸和蛋白质(肽)链的新型酰胺耦联反应“二酰基二硫化物耦联(DDC)”。
然后利用基于DDC的合成法,开发出了可将糖链自由插入蛋白质的任意位置的糖蛋白合成法。
由此可以将合成的糖链迅速嵌入糖蛋白,从原料开始大约只需5步就能成功合成出高纯度糖蛋白。
研究团队还测量了IL3(拥有用此次开发的方法合成的糖链)的细胞增殖活性,评估了糖链的功能,由此发现了促进IL3与其受体蛋白结合的新作用机制。
为了研究此类糖链作用影响的实验,必须快速获得具有均一糖链的高纯度糖蛋白,这种合成法被认为将成为今后探究糖蛋白上的糖链功能的关键。
另外,利用这种合成法可以快速制备糖蛋白,还有望应用于糖蛋白制剂。
梶原教授表示:“糖蛋白的化学合成大约20年前就开始了。当时完全无法实用化,只是在实验室中勉强能合成。此次的合成研究是2015年前后开始与野村、毕业生原口以及冈本讲师和真木助教等人一起推进的,从意外发现的肽合成法中发展而来。虽然还需要进行改良,但只需几个步骤就能合成糖蛋白是一项超出预期的成果,今后还可以用于新药研发。”
原文:《科学新闻》
翻译编辑:JST客观日本编辑部













