本文根据冈山大学成果发布编译整理而成
冈山大学医院新医疗研究开发中心再生医疗部的王英正教授与该大学医院儿科的平井健太医生等人,通过对扩张型心肌病猪模型及小儿扩张型心肌病1)患者实施心脏内干细胞移植发现,已陷入心力衰竭的心脏功能可以恢复。尤其是发现,移植的细胞内分泌的细胞外囊泡中,名为miR-146a-5p的微RNA能直接发挥抗炎作用,从而防止受损的心脏组织纤维化,还有助于预测治疗效果。
扩张型心肌病是最常见的小儿心肌病,确诊后5年内能避免心衰死亡或心脏移植的几率约为50~60%,是一种预后非常差的心脏病。除器官移植外,细胞移植也是备受期待的治疗方法之一,但目前尚无有用的大型动物实验模型,研究开发没有太大进展。
研究成果
此次,研究团队通过向猪心脏表面的冠状动脉内注入100~300微米的微颗粒,全球首次成功培育出40头心脏整体的功能显著下降的扩张型心肌病猪模型。移植心脏内干细胞时,采用了安全性更高的不切断冠状动脉血流的移植法(non stop-flow technique),而不是以前常用的临时切断冠状动脉血流的方法(stop-flow technique)。试验确认,通过向冠状动脉内注入干细胞,降低的心脏功能明显得到改善,病理组织显示新生成了心肌和血管细胞,同时受损组织的纤维化区域明显减小。研究团队详细分析移植的猪心脏内干细胞发现,分泌了细胞外囊泡,其中含有6种对心肌保护和血管新生至关重要的微RNA(图1上)。
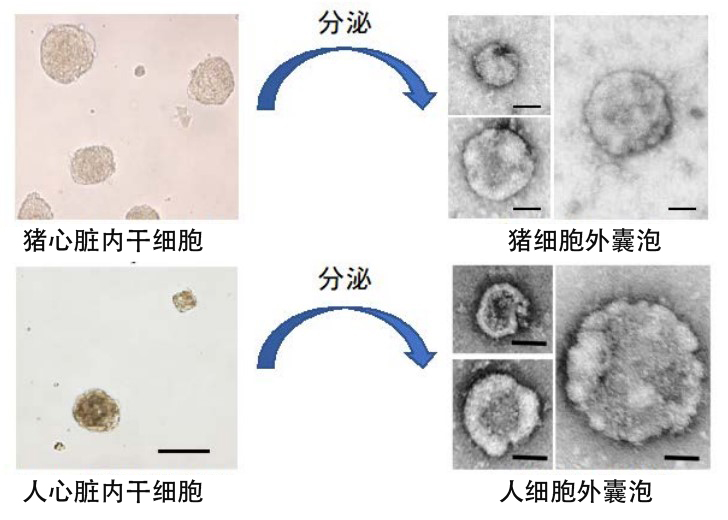
图1:细胞外囊泡含有多种具备抗炎作用的微RNA,由心脏内干细胞分泌。
另外,临床研究还连续针对5例心脏泵血功能降至40%以下(通常心脏泵血功能达到65%以上属于正常)的小儿扩张型心肌病患者纯化并大量培养了来自患者本人的心脏内干细胞,然后实施了自体干细胞移植。虽然有一例出现副作用,但全部5位患者均安全实施了移植,且最终结果证明治疗取得了效果。此次的临床研究是利用心脏内干细胞治疗小儿扩张型心肌病的细胞移植法的全球首例报告。
研究还确认,从猪模型中检测出来的6种微RNA在源自患者本人的心脏内干细胞的细胞外囊泡中均大量存在(图1下)。尤其是发现,miR146a-5p的表达量与移植患者的心脏功能恢复程度具有明显的相关性。研究团队向人的心肌细胞中实验性地导入miR-146a-5p发现,可抑制3种重要的炎症性细胞因子的产生,能强烈抑制心肌细胞死亡和组织纤维化,由此确认了上述临床现象。
利用此次的研究成果,有望开展旨在使心脏内干细胞移植适用保险的二期临床试验,今后将针对此前只能通过心脏移植挽救生命的严重小儿扩张型心肌病,开发可作为新医疗方法提供的技术并完善实施体制。
名词解释
1. 小儿扩张型心肌病
由于心肌的收缩力下降,导致心脏壁变薄且心室腔大幅扩大的疾病。约50~70%的病因尚不清楚,组织病理显示心肌细胞发生变性和纤维化。据报告,部分家族性病例的细胞骨架蛋白出现基因异常,但普通的病毒性感冒引起的心肌炎也可能引发此病。临床症状表现为心律失常、心力衰竭和猝死,婴幼儿和年轻人的预后尤其差,属于儿童慢性特定疾病。
论文信息
题目:Cardiosphere-derived exosomal microRNAs for myocardial repair in pediatric dilatedcardiomyopathy
期刊:Science Translational Medicine
DOI:10.1126/scitranslmed.abb3336
日语发布资料
编译:JST客观日本编辑部














