本文及图片均摘抄编译自顺天堂大学的研究成果公关发布资料
日本顺天堂大学的奥村康特任教授和内田浩一郎副教授主导的研究团队,向独立行政法人医药品医疗机器综合机构(PMDA)提交了实施“评估诱导型抑制性T细胞(以下简称JB-101)在活体肝移植中的免疫耐受诱导能力及安全性的I/II期临床试验”申请,将启动由医生主导的临床试验。
顺天堂大学的研究团队发现了选择性地抑制对供体器官的免疫排斥反应的T淋巴细胞(JB-101),可长期诱导名为免疫耐受的非排斥状态,并于2016年利用诱导型抑制性T细胞成功地让肝移植患者完全脱离了免疫抑制剂。另外,2019年通过与顺天堂大学创办的新药开发初创企业JUNTEN BIO开展联合研究,还成功确立了稳定制造诱导型抑制性T细胞“JB-101”的方法。此次,顺天堂大学将在日本移植学会的支持下,联合东京女子医科大学、广岛大学和长崎大学共同实施由医生主导的评估JB-101的有效性和安全性的临床试验,以实现无需使用免疫抑制剂的肝移植疗法。
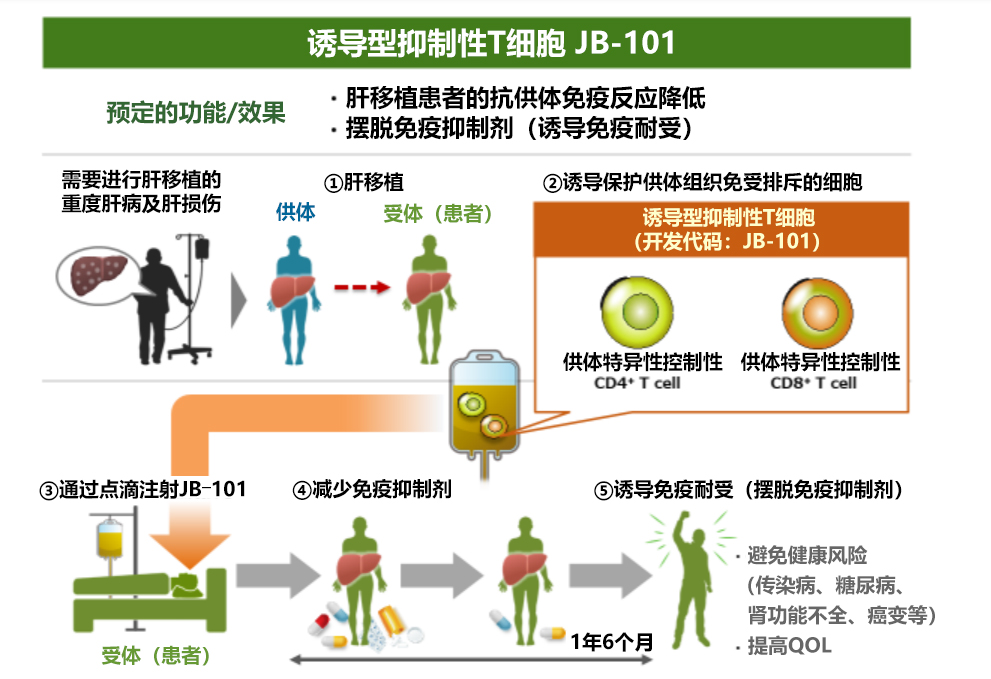
图1:关于JB-101的免疫耐受诱导
临床试验概要
此次临床试验征得患者同意后将在实施肝移植前的观察期进行筛查,以确认是否适合参加临床试验,然后利用单采术(Apheresis)在实施肝移植的14天前~3天前从供体、在实施肝移植的前一天从受试者体内采集外周血单核细胞。将从供体和受试者体内采集的白细胞中的单核细胞与CD80/CD86抗体(激活T细胞的分子)进行共培养,培养的单核细胞会转化成保护供体组织免受排斥的细胞(诱导型抑制性T细胞“JB-101”)。
作为注射JB-101的预处理,为暂时减少体内的淋巴细胞,在实施肝移植后的第五天投用环磷酰胺。然后在实施肝移植10天或11天后为患者注射JB-101,利用约1年零6个月的时间慎重观察是否会发生排斥反应,并逐渐减少免疫抑制剂的用量,最终彻底停用免疫抑制剂(摆脱免疫抑制剂)。
临床试验把摆脱免疫抑制剂超过1年以上的情况定义为“免疫耐受”,将评估JB-101的效果。临床试验的结果将提交给厚生劳动省进行审查。如果确认效果和安全性没有问题,将作为再生医疗等的产品通过审批(计划2026年内实现实用化)。该临床试验的目标是使顺天堂及日本的再生医疗技术实现实用化,作为向全球推广的第一步。
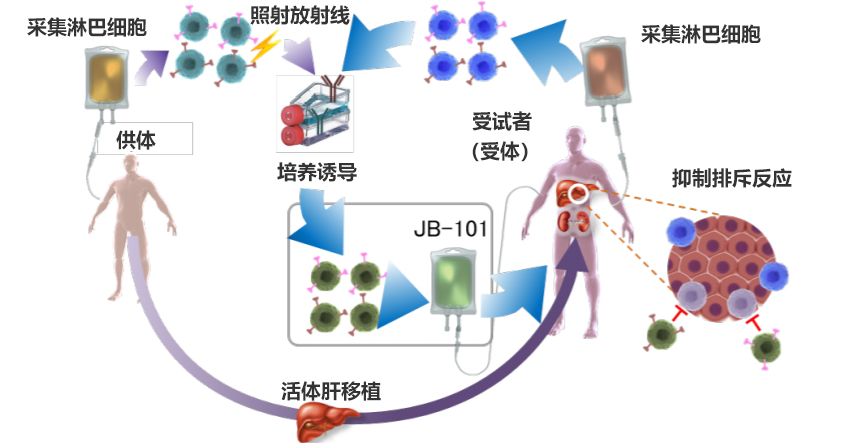
图2:JB-101的制造流程
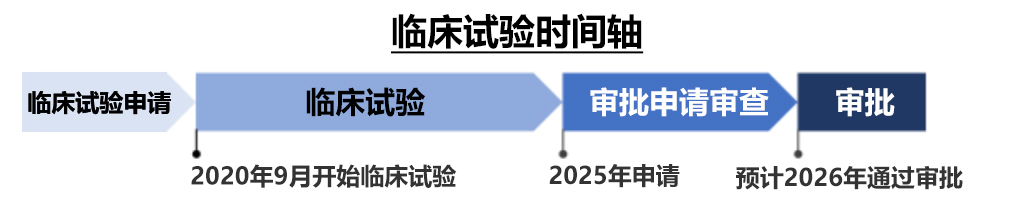
图3:该临床试验的时间轴(目前的计划)

图4:该临床试验的实施体制
公关发布资料
编译:JST客观日本编辑部














