作为抗血小板凝聚药物广泛使用的阿司匹林的抗肿瘤效果近年来也备受关注,成为以预防和治疗癌症为目的的药物重定位的最有力候补。不过,阿司匹林的副作用,如消化性溃疡和出血倾向等也不容忽视,因此业界正全力探索能提前预测阿司匹林抗肿瘤效果的生物标志物,以及开发旨在更安全有效地提高阿司匹林抗肿瘤效果的联用治疗药物。
在这一过程中,随着癌症基因组解析的进步,阿司匹林的抗肿瘤效果与癌症基因组之间的关系变得明确,尤其是对于占大肠癌10~20%的PIK3CA基因突变大肠癌,近年来接连报告了证明阿司匹林高度有效的临床数据。不过目前还不清楚其详细机制,全球正在对此开展基础研究。
另一方面,已知癌细胞不同于正常细胞,各种代谢路径的异常会支持细胞过度繁殖,在PIK3CA基因突变癌细胞中,氨基酸代谢之一的谷氨酰胺代谢也被激活,对此,京都府立医科大学和关西医科大学的研究团队假设“PIK3CA基因突变引起的谷氨酰胺代谢增强可能会影响阿司匹林的敏感性”,并推进了相关研究。
研究内容和成果的要点
首先,研究团队验证了阿司匹林的效果预测因子——PIK3CA基因突变发生与否,以及细胞培养液中有无谷氨酰胺是否会影响阿司匹林抑制细胞繁殖的效果。结果发现,在发生PIK3CA基因突变的大肠癌细胞中,去除培养液中的谷氨酰胺后,对阿司匹林的敏感性会降低(图1)。
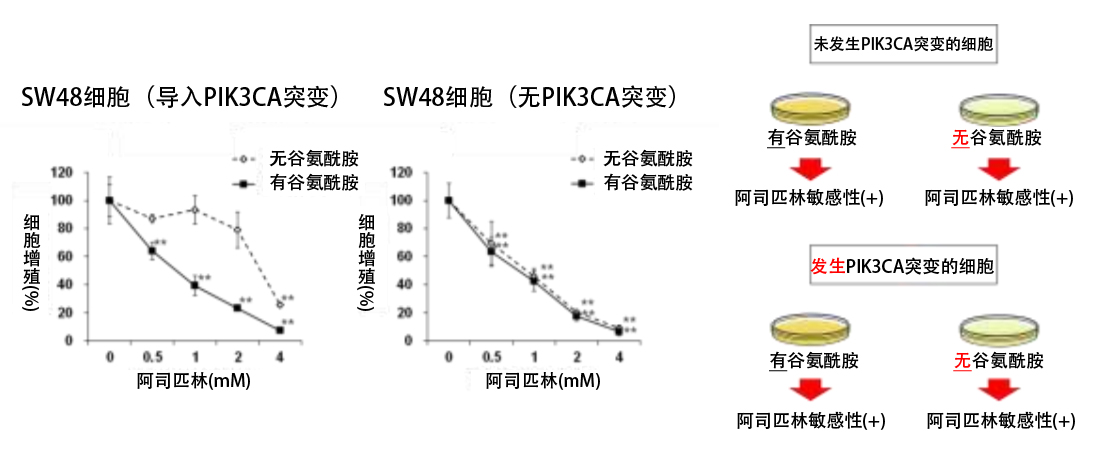
图1:利用PIK3CA突变(±)SW48细胞分别在培养基中有谷氨酰胺和没有谷氨酰胺的情况下比较了阿司匹林的抗肿瘤效果,发现仅在PIK3CA突变细胞中,去除谷氨酰胺会降低对阿司匹林的敏感性。
接下来利用分子生物学方法确认,去除培养液中的谷氨酰胺时诱导的氨基酸代谢的主调节因子——转录因子ATF4在添加阿司匹林时也会被诱导表达。这表明,阿司匹林可能会促进癌细胞吸收谷氨酰胺。因此,研究团队利用综合基因解析法 (RNA-seq)解析了阿司匹林处理对基因表达的影响,发现与掌管细胞吸收氨基酸的转运蛋白有关的基因簇表达出现了增加(图2)。
图2:利用新一代测序仪对癌细胞全面进行基因解析(RNA-seq)确认,阿司匹林会激活与谷氨酰胺代谢有关的基因。
另外还发现,利用阿司匹林处理后,多种与谷氨酰胺代谢有关的酶的表达增强,由此得出一个以前不知道的新发现,即“阿司匹林通过诱导ATF4表达,会激发癌细胞内的谷氨酰胺代谢”。为将阿司匹林用于癌症预防和治疗,研究团队同时使用阿司匹林和多种谷氨酰胺代谢抑制剂,对PIK3CA大肠癌细胞进行了长时间(1周)处理,发现了对抑制癌细胞集落的形成具有协同抑制效果。
这表明,被阿司匹林激发的谷氨酰胺代谢通过氧化应激诱导耐受性和能量代谢回路的活性,对癌细胞的存活产生了重要意义,同时也表明,阿司匹林和谷氨酰胺代谢抑制剂联用的治疗方法与单独使用阿司匹林治疗相比,可能是更有效的治疗方案(图3)。
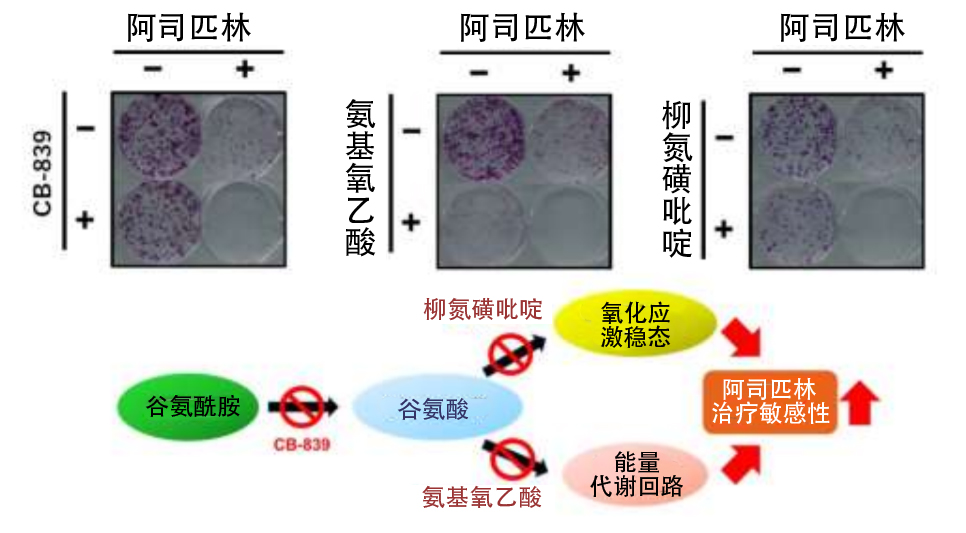
图3:通过药剂抑制阿司匹林激活的谷氨酰胺代谢,能与阿司匹林发挥出协同抗肿瘤效果。
结论
本研究表明,在PIK3CA突变大肠癌中,如果缺乏谷氨酰胺,阿司匹林就无法充分发挥抗肿瘤效果。
另外,本次研究还从分子机制上证明了阿司匹林会激活谷氨酰胺的代谢。而通过抑制被阿司匹林激活的谷氨酰胺代谢,则有望提高阿司匹林的抗肿瘤效果。
论文信息
题目:Deactivation of Glutaminolysis Sensitizes PIK3CA-Mutated Colorectal Cancer Cells to Aspirin-Induced Growth Inhibition
期刊:《Cancers》
DOI编号:2072-6694/12/5/1097
文:JST客观日本编辑部














