日本国立研究开发法人国立癌症研究中心东医院,以接受大肠癌(结肠/直肠癌)外科治疗的患者为对象,启动了旨在通过检测血中循环肿瘤DNA(ctDNA)的技术(液体活检)实现癌症精准医疗的项目“CIRCULATE-Japan”(研究代表:东医院消化道内科长吉野孝之)。
CIRCULATE-Japan将利用产学合作全国癌症基因组筛查项目“SCRUM-Japan”,以肉眼看不见的癌症(术后微小残留病变)为对象,实施全球最大规模的、由医生主导的跨国联合临床试验,国内外共有约150座设施(包括台湾的1座设施)参加。临床试验以预定实施根治性手术治疗的约2,500名大肠癌患者为对象,将确定各位患者因癌症引起的基因异常,并为每位患者制作基因面板,然后定期采血,调查是否存在基因异常。

CIRCULATE-Japan的定位
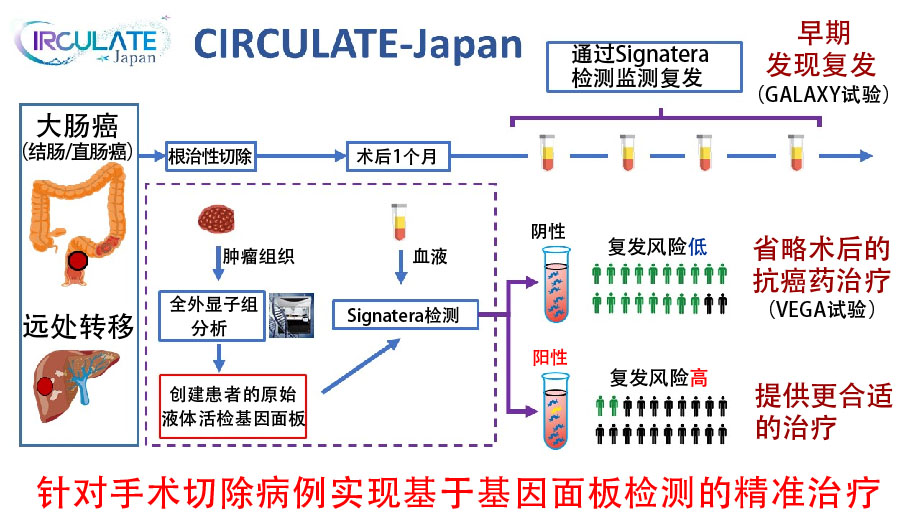
CIRCULATE-Japan项目概要
国立癌症研究中心东医院的院长大津敦表示:“CURCULATE-Japan是一项划时代的研究,可利用最新的液体活检技术,为术后需要使用抗癌药物辅助化疗的患者筛选合适的治疗方法,日本有望引领世界,实现癌症治疗整体的范式转变。”
以前,大肠癌的标准治疗方法是,实施手术切除后,为预防复发会根据按病期推算的复发风险,进行术后辅助化疗。不过,药物的效果和副作用因患者而异,尤其是会留下周围神经病变(四肢麻木)等后遗症问题。该项目计划利用美国Natera公司开发的高灵敏度基因解析技术“Signatera”检测法,以更高的精度推算每位患者的术后复发风险。
如果能通过CURCULATE-Japan证明液体活检的复发风险评估精度及其临床有用性,则可以只筛选术后辅助化疗法更有望取得效果的患者,由此能避免不必要的治疗,从而降低副作用和后遗症的风险。另外,这种检测法可通过身体负担较小的采血反复测量,有望更早发现癌症复发。
通过本次研究获得的癌症基因组信息及临床信息将作为大规模数据库进行整合,有助于研究开发新的癌症诊断方法和治疗药物。另外,为了与全国的医疗机构和企业合作,同时推进多个临床试验,将与EPS控股公司共同运营项目。计划建立适合新的临床研究开发基础的支援体制,推进该项目顺利进行。
研究背景
可以外科治疗的大肠癌一般采用手术的方式来治愈癌症。另外,还会根据手术的病理组织检测判断癌症的术后病期,由此推算复发风险,并实施术后辅助化疗。但目前存在的问题是,光根据病期推算复发风险会让那些本来没必要与高复发风险患者接受相同治疗的患者也接受相同的治疗。
近年来,作为更精确的癌症复发风险推算手段,业界正在研发利用采集的血液解析血中循环肿瘤DNA(ctDNA),并将其应用于诊断治疗的“液体活检”。美国Natera公司开发的超高灵敏度基因解析技术“Signatera”检测法有望推算术后的复发风险及早期发现复发。
日本国立癌症研究中心于2015年2月启动了产学合作全国癌症基因组筛查项目“SCRUM-Japan”,以难以实施手术切除的实体癌患者为对象,推进了调查癌症基因异常的项目。目前,全国已有200多家医疗机构及17家制药企业和诊断药企业参加该项目,学术界、临床现场和产业界齐心协力,共同推进了适合日本癌症患者的基因异常的治疗药物和诊断药物的开发。
此次又利用SCRUM-Japan打下的基础,在国内外约150座设施的协助下,启动了旨在为接受外科手术治疗的大肠癌患者提供最佳治疗方案的新项目CIRCULATE-Japan。
1. 实施由医生主导的全球最大规模国际联合临床试验
2020年5月8日开始以能进行根治性手术治疗的结肠/直肠癌患者为对象启动注册研究(GALAXY试验)的注册工作。日本国内外约150座设施(包括台湾的1座设施)参加了该研究。
本次研究以预定接受根治性手术治疗的约2,500名2期至4期大肠癌患者为对象,将在术后2年内,实施利用液体活检监测复发情况的检测(Signatera检测)。计划根据手术中取出的肿瘤组织的全外显子解析结果,为患者制作原始的基因面板。然后从术后1个月开始定期采血,利用每位患者的原始基因面板,调查血液中是否存在癌症基因异常。
此外,以术后1个月时未检测出癌症基因异常的1,240名2期至3期患者为对象,对常规的标准治疗——术后辅助化疗组和随访组进行比较的三期临床试验(VEGA试验)也同时开始注册。
2. 建立新的临床研究开发基地
该项目通过与临床试验联动,可以同步开发针对更多患者的新诊断治疗法。要想建立这种大规模且复杂的临床试验实施体制,学术界与研究支援企业必须紧密合作。另外,为确保通过长期随访获得的宝贵临床信息和基因信息的品质并顺利推进项目,EPS控股公司与国立癌症研究中心签订了联合研究协议,计划建立适合这种新的临床研究开发基础的新支援体制。
【实施时间】
研究时间:2020年4月1日~2030年3月31日
【目标病例】
预定接受根治性手术治疗的结肠/直肠癌(包括向其他器官远处转移的患者)
【目标病例数量】
2,500例
【解析方法】
利用Natera公司的Signatera™筛查血中循环肿瘤DNA(ctDNA)
【参加的医疗机构】
截至2020年6月2日
日本国内 145座设施(包括正在准备中的设施)
台湾 1座设施
【参加的企业】
截至2020年6月2日,已经签订联合研究协议的企业
EPS控股公司:支援GALAXY/VEGA试验的运营工作
SRL公司:样本的管理、运输和保管等
TeDaMa公司:提供和创建数据收集环境,并在数据收集时进行操作
Falco Biosystems公司:资材搬入、MSI检测与预后信息的综合分析
Natera公司(美国):实施Signatera检测
文:JST客观日本编辑部














