东京大学研究生院药学系研究科的富田泰辅教授、堀由起子讲师和邱咏玟研究生等人,与新潟大学脑研究所的池内健教授等人组成的研究团队,在利用创新技术调查脑功能网络全貌项目“阿尔茨海默病的Aβ诱导性tau凝集病态传播与神经回路变化机制调查”(JP20dm0207073)的支援下,通过采用CRISPR/Cas9系统的全基因组筛查,查出了与产生Aβ有关的新分子,并由此确定钙整合素结合蛋白1(Calcium and Integrin-Binding Protein 1:CIB1)是对Aβ的产生有负调控作用的新分子,同时还明确了调控Aβ的机制(图1)。另外研究团队还发现,早期阿尔茨海默病(AD)患者死亡后大脑中的CIB1表达量出现了下降。
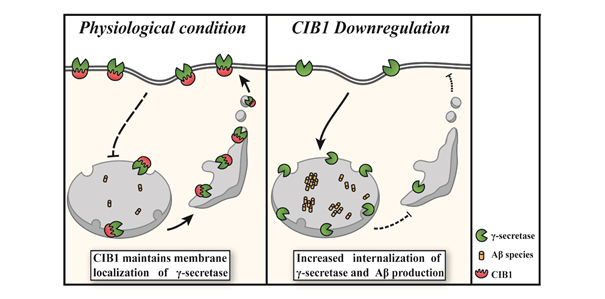
图1:CIB1调控Aβ产生的机制
研究发现,CIB1将γ分泌酶留在了细胞表面膜上(左图)。在以往的研究中人们已经知道,γ分泌酶的亚细胞定位会影响其裂解活性。也就是说,CIB1的表达量减少时,细胞表面上的γ分泌酶表达量会下降,Aβ就会出现增加(右图)。
在当今的老龄化社会,占老年痴呆症大部分病例的阿尔茨海默病(AD)已成为严重的社会问题,但目前尚未完全明确其发病机理,也没有确立根治方法。AD早期表现出的病理学特征是,β-淀粉样蛋白肽(Aβ)在大脑中的聚集和积累。此前实施的大量遗传学研究表明,Aβ的聚集和积累会在神经细胞内引起tau的聚集和积累,从而引起神经变性。因此,了解Aβ的具体产生机制被认为有助于查清AD发病的早期过程。
Aβ是淀粉样前体蛋白(APP)被β分泌酶和γ分泌酶分两阶段裂解而产生的。其中γ分泌酶的裂解根据其裂解位点的不同会为Aβ的C末端带来多样性,并参与跟AD发病有关的高聚集性Aβ分子的产生,因此γ分泌酶的活性调控被认为是治疗AD的重要靶标。不过,关于其裂解调控机制一直存在很多不明之处。
此次研究团队为确定与Aβ产生有关的新分子,利用近年来开发的基因编辑技术CRISPR/Cas9系统,实施了全基因组筛查。由此成功确定钙整合素结合蛋白1(Calcium and Integrin-Binding Protein 1:CIB1)是对Aβ产生有负调控作用的新分子。敲低或敲除CIB1减少蛋白质含量,Aβ的产生量出现了增加。
关于其机制,研究团队通过免疫共沉淀实验发现CIB1与γ分泌酶存在相互作用。另外还发现,CIB1不会影响γ分泌酶的总量,但会影响γ分泌酶在细胞表面膜的存在量。这表明,CIB1在生理条件下会与γ分泌酶相互作用,将γ分泌酶留在细胞膜上(图1左)。另一方面,研究认为,当CIB1的表达量减少时,这个功能会消失,γ分泌酶的内化增强(图1右)。此前的研究发现,γ分泌酶的亚细胞定位会影响其裂解活性。也就是说,CIB1通过改变γ分泌酶的亚细胞定位来调控Aβ的产生。
为研究CIB1在AD发病过程中的作用,研究团队解析了人类AD患者死亡后的脑样本单细胞RNA测序数据。解析结果发现,在早期AD阶段的神经细胞中,CIB1的表达量减少。这些结果表明,神经细胞中的CIB1表达量减少可能会增加Aβ的产生量,并加速AD的发病进程。
此次研究成功确定了与Aβ产生有关的新分子,并明确了部分产生调控机制,是一项极为有意义的成果。另外研究还发现,在AD发病的早期阶段,CIB1的表达变化会改变γ分泌酶的亚细胞定位,增加Aβ的产生,从而加速AD的发病进程。今后有望以CIB1为靶标制定新的AD治疗和预防战略,以及开发早期诊断法。
论文信息
题目:Identification of calcium and integrin-binding protein 1 as a novel regulator of production of Amyloid β peptide using CRISPR/Cas9-based screening system
期刊:《The FASEB Journal》
DOI:10.1096/fj.201902966RR
文:JST客观日本编辑部














