日本金泽大学纳米生命科学研究所及癌症进展控制研究所的中山瑞穗助教和大岛正伸教授,与首尔大学的Seong-Jin Kim教授组成的联合研究团队,成功查清了p53基因的特异性突变模式促进大肠癌肝转移的机制。
抑制癌细胞增殖的p53基因被认为是重要的“抑癌基因”,在很多癌症中都发现该基因发生了突变,其功能缺损会促进癌变。另一方面,还有报告显示,通过氨基酸突变获得新功能的突变型p53会积极促进癌变。这种突变被称为功能获得(Gain-of-Function:GOF)型突变。研究团队开发出了通过移植源自小鼠大肠癌的类器官来再现人类大肠癌肝转移的模型,发现同时发生p53功能缺损和GOF型突变会诱导转移灶的形成。
【研究背景】
癌症被称为基因病,是由基因突变的积累引起的。其中,抑制癌细胞增殖的p53基因在很多癌症中都发生了突变,是重要的“抑癌基因”。另一方面,已知氨基酸序列随着基因突变而发生变化的突变型p53会获得新的促癌功能,被称为功能获得(Gain-of-Function:GOF)型突变。不过,关于p53原本具备的抑癌功能的缺损与发生GOF型突变的p53的作用是如何相互关联并促进癌变和病情恶化的,此前并没有相关报告。人类一直未能开发出再现体内癌细胞恶化情况的模型被认为是研究没有取得进展的主要原因之一。
【研究成果概要】
此次,研究团队此前在小鼠肠道上皮细胞中导入了会引发大肠癌的4种重要基因突变,培养了具备转移能力的类器官。构成类器官的癌细胞在等位基因染色体单侧的p53基因中导入了GOF突变,另一侧则保留了野生型p53基因。通过将类器官移植到小鼠身上并解析形成的肝转移灶发现,缺少野生型p53基因的癌细胞会选择性地转移复发(图1)。
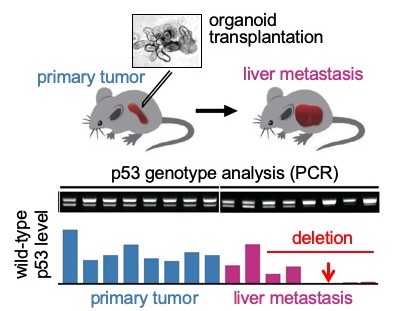
图1:转移到肝脏的癌细胞的基因分析结果
将源自大肠癌的类器官移植到小鼠的脾脏中(上),对转移到肝脏的癌细胞的p53基因状态实施了PCR解析。结果显示,转移的癌细胞大部分都缺少野生型p53(下)。
另外,研究团队解析类器官发现,表达GOF型突变p53且缺少野生型p53基因的癌细胞,类器官的结构显著发生变化,在转移组织中的存活率明显提高,这种现象被认为会促进转移灶的形成。此外,基因表达解析显示,上述特异性p53突变模式可能会诱导与干细胞特性及炎症和增殖有关的信号增强,从而促进癌细胞转移(图2)。
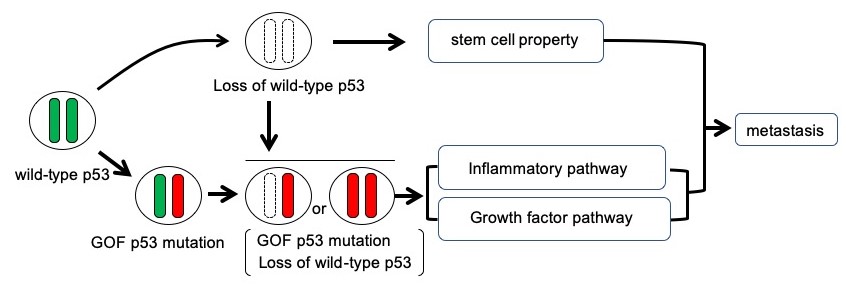
图2:p53突变模式与癌细胞转移的关系
缺少野生型p53且p53发生GOF型突变被认为会诱导与干细胞特性的获得及炎症和增殖有关的信号增强,从而促进癌细胞转移。
不仅是大肠癌,很多癌组织中都检测出p53发生GOF型突变,恶性化的癌细胞中缺少野生型p53。这些现象被认为与癌症的恶性化有关,本研究首次确认,这些现象的相互作用是促进癌细胞转移的关键。
【未来展望】
上述发现表明,通过抑制突变型p53的功能,也许能抑制癌细胞转移,有望用来开发预防和治疗大肠癌转移的新药。
论文信息
题目:Loss of wild-type p53 promotes mutant p53-driven metastasis through acquisition of survival and tumor-initiating properties
期刊:《Nature Communications》
DOI:10.1038/s41467-020-16245-1
文:JST客观日本编辑部














