日本量子科学技术研究开发机构的平野俊夫理事长与北海道大学遗传病控制研究所的村上正晃教授共同指出,感染新型冠状病毒(COVID-19)后出现的急性呼吸窘迫综合征(ARDS: Acute Respiratory Distress Syndrome)实为细胞因子风暴引起的细胞因子释放综合征(CRS: Cytokine Release Syndrome),IL-6-STAT3通路可作为预防这种综合征的治疗靶标。
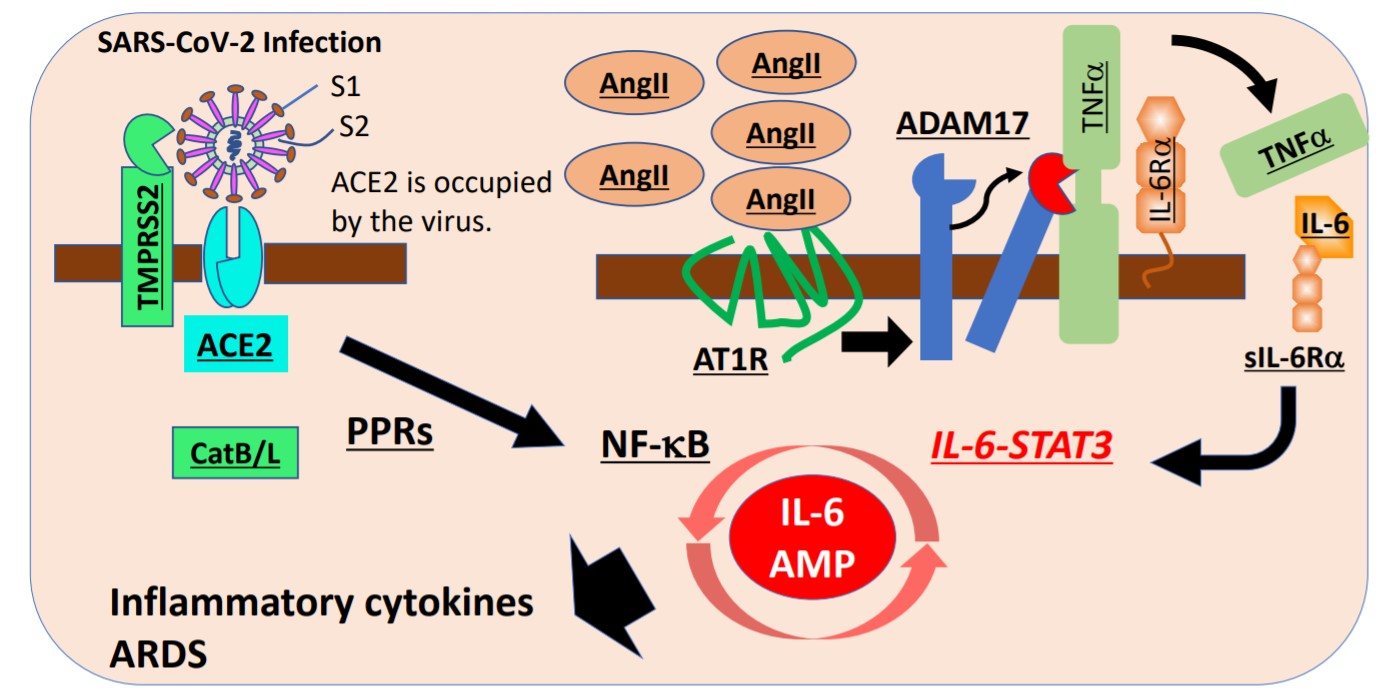
感染SARS-CoV-2时,支气管和肺泡上皮细胞中的IL-6增幅器(IL-6 Amplifier)被激活,诱发细胞因子过度产生并出现急性呼吸窘迫综合征(ARDS)的模式图
在支气管和气道上皮细胞中与ACE2结合的SARS-CoV-2病毒会在TMPRSS2的作用下进入细胞内。然后激活识别病毒分子结构的细胞模式识别受体(PPRs),进而激活下游的NF-kB通路。另外,随着病毒的感染,原本与ACE2结合并被分解的血管紧张素(AngII)在血液中增加,来自血管紧张素受体1(AT1R)的信号变得过剩。
被激活的AT1R信号会激活蛋白质分解酶ADAM17,将细胞膜形态的TNFa、IL-6Ra和生长因子等炎症相关分子变成可溶性分子。可溶性TNFa和IL-6-可溶性IL-6Ra(sIL-6Ra)在包括支气管和肺泡上皮细胞及血管内皮细胞的非免疫系统细胞中会同时激活NF-kB和STAT3,从而激活过度的NF-kB活性化机构IL-6增幅器,导致这些细胞局部产生过剩的细胞因子。由此引起细胞因子释放综合征CRS,最终引发COVID-19出现的致命性急性呼吸窘迫综合征ARDS。
COVID-19患者出现的致命性急性呼吸窘迫综合征ARDS属于细胞因子释放综合征CRS,如果能治疗CRS,新型冠状病毒将变得不再可怕。有望用来开发治疗药物的靶标包括TMPRSS2、ACE2、AT1R、ADAM17、TNFa以及在IL-6增幅器中发挥重要作用的IL-6-STAT3通路等。尤其是在感染后期出现的致命性ARDS的治疗,还有望利用已用于CAR-T治疗中的CRS治疗,而且可抑制IL-6增幅器的抗IL-6受体抗体。
论文信息
COVID-19: a new virus, but an old cytokine release syndrome
(https://marlin-prod.literatumonline.com/pb-assets/products/coronavirus/immuni4349_S5.pdf)
文:JST客观日本编辑部














