日本京都工艺纤维大学分子化学系的北所健悟副教授等人组成的研究团队,通过与大阪府立大学综合康复学研究科的神谷重树教授、京都大学医学研究支援中心的奥野友纪子特定讲师、理化学研究所放射光科学研究中心利用系统开发研究部门的引间孝明研究员及山本雅贵部门主任等开展联合研究,利用X射线结构解析法,全球首次查清了金黄色葡萄球菌产生的毒性因子之一“脂肪酶(SAL)”的立体结构。
另外研究团队还发现,作为抗肥胖药物销售的人类脂肪酶抑制剂“奥利司他”与现有的SAL抑制剂相比,抑制SAL活性的效果达到200倍以上。此外,通过在原子水平解析SAL与奥利司他的复合体的结构,成功查清了奥利司他的抑制机制。
这项研究成果有助于推进基于结构信息的SAL药物的理论开发,有望实现效果更高、副作用更少的治疗药物的探索和设计。特别是,SAL与金黄色葡萄球菌的增殖有关,因此还有望开发出针对现有抗菌药无效的MRSA传染病以及金黄色葡萄球菌引起的特应性皮炎等的治疗药物。
研究背景
全球的医院中都存在现有抗菌药无效的细菌“超级细菌”,其流行令人担心。MRSA(耐甲氧西林金黄色葡萄球菌)就是超级细菌的代表,由于其对各种抗菌药都表现出耐药性,名为MRSA感染的院内感染已成为严重问题。金黄色葡萄球菌(Staphylococcus aureus:以下简称SA菌)是化脓的伤口和皮肤表面存在的常居菌,会通过伤口进入体内,并产生大量毒力因子,引起各种疾病。研究发现,在有多种细菌存在的皮肤表面,SA菌异常增加会引起特应性皮炎。SA菌产生的毒力因子之一“脂肪酶(SAL)”与SA菌的增殖有关,通过分解具有源自免疫反应的杀菌效果的脂质,提高细菌的存活率,会破坏生物防御。因此,不仅是抗MRSA药物的靶标,SAL抑制剂作为治疗特应性皮炎的药物也备受关注。
为推进效果更高、副作用更少的新药探索和设计,此次研究试着运用此前利用大型同步辐射设施“SPring-8”的强同步辐射实施X射线结构解析的经验,调查了SAL的立体结构。
研究内容
刚开始研究时没有任何关于SAL立体结构的信息。另外,针对SAL的抑制剂也没有活性较强的有效产品。因此,研究团队首先探索了SAL抑制剂,发现作为抗肥胖药物已在海外获批的奥利司他(图a)能以2.4μM的IC50值抑制SAL。另外发现,奥利司他的抑制活性达到此前已知的SAL抑制剂法尼醇的200倍以上。
在此次研究中,为利用X射线晶体结构解析法在原子水平查清奥利司他分子与SAL结合形成的复合体的立体结构,研究团队首先利用大肠杆菌构建了SAL的大量生产体系。纯化高纯度SAL,制作了SAL单体的晶体与奥利司他共结晶的晶体。X射线衍射实验和数据收集利用大型同步辐射设施“SPring-8”的光束线BL41XU及BL44XU实施。
SAL的立体结构是与现有的其他细菌的脂肪酶非常相似的三维结构,呈开放式构象,具有覆盖活性位点作用的Lid结构域为开放状态(图b)。研究发现,奥利司他分子作为“钥匙”分子,与SAL的活性位点“钥匙孔”完全嵌合(图c)。
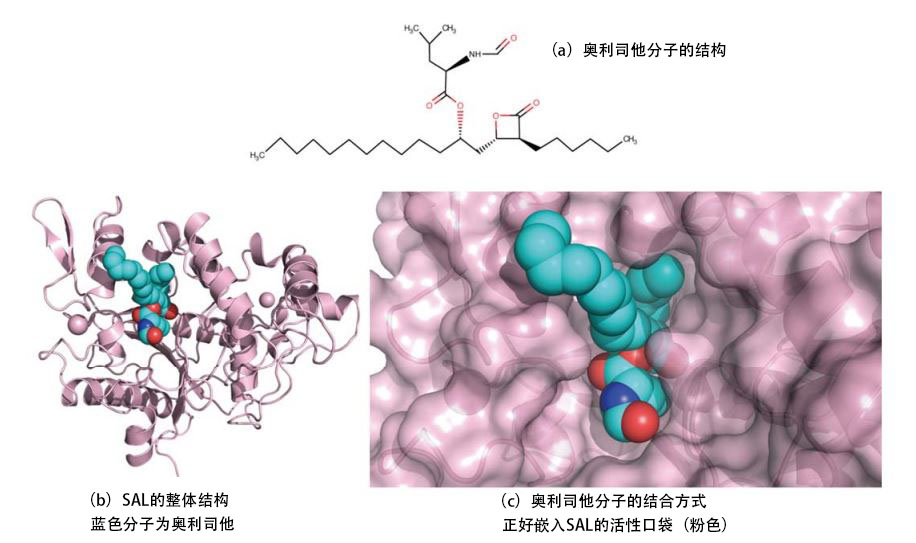
另外,奥利司他是相对比较大的分子,与SAL的催化残基——第116个丝氨酸残基的氧原子共价键合。其他两个部分以疎水性相互作用的形式存在于SAL相对较宽大的活性位点——口袋里。这些结合方式表明,奥利司他对SAL具有较高的选择性亲和性。通过此次的成果,确立了通过药物设计推进药物开发的基础知识。
社会意义与未来展望
研究团队通过奥利司他与SAL的相互作用,构建了进行药物设计的结构基础。已知MRSA对大多数抗菌药都产生了耐药性,会造成新生儿和老人等免疫力较差的患者死亡。
探索针对MRSA的非抗菌药物非常重要,SAL抑制剂作为针对MRSA感染的具有新作用机制的药物备受期待。此次的研究结果有望以SAL为靶标,针对MRSA和皮肤病等疾病,开发基于其结构信息的新药(Structure based drug design)。另外,奥利司他在海外已经通过审批,因此作为药物重定位,药物适用范围有望扩大到感染症领域。
论文信息
题目:Crystal structure of pathogenic Staphylococcus aureus lipase complex with the anti-obesity drug orlistat
期刊:《Scientific Reports》
DOI:10.1038/s41598-020-62427-8
文:JST客观日本编辑部














