日本理化学研究所(简称“理研”)的主任研究员田中克典和特别研究员野村昌吾等人组成的研究团队,通过在细胞上合成人工糖肽,成功地像指纹认证一样对癌细胞进行了模式识别,并利用该模式标记了小鼠体内的特定癌组织。

图1:左起分别为田中克典主任研究员和野村昌吾特别研究员
2017年,田中主任研究员等开发了利用RGDyK肽与细胞表面的整合素之间“强”相互作用,以及糖链与受体凝集素之间“弱”相互作用的细胞识别技术。
此次,研究团队对该项技术进一步开发,发现通过组合4种RGDyK肽和5种糖链,并利用点击反应在细胞上合成人工糖肽,能对5种癌细胞和1种非癌细胞进行模式识别。另外,团队还利用建立的模式识别了小鼠体内的癌组织,成功高灵敏选择性地识别出特定的癌组织。
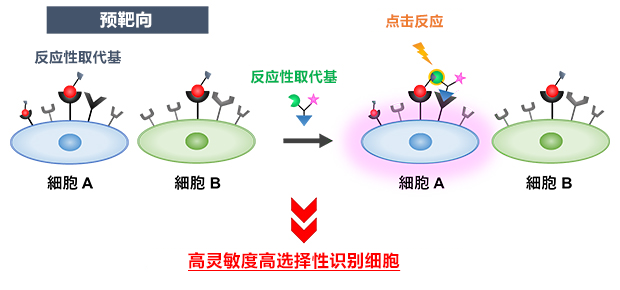
图2:组合2种分子识别靶细胞
研究背景
人和动物等体内分子成像作为选择性识别抗癌药物的体内动态和特定细胞的诊断方法备受关注。以往的分子成像广泛使用与目标识别的靶细胞表面表达的1种受体“强”相互作用的低分子化合物、抗体及肽等配体分子。
但利用“强”相互作用的配体分子的话,由于其与靶细胞以外的细胞中表达的受体也会“强”相互作用,因此从大量细胞中选择性地识别靶细胞的能力有限。例如,想利用“强”相互作用的配体分子。从表达相同种类受体的细胞A和B中仅选择性地识别细胞A时,由于配体分子与细胞A和B的受体都会相互作用,因此很难区别两种细胞(图3a)。另外,利用“弱”相互作用的配体分子的话,即使与受体相互作用也会立即分离,所以无法以高灵敏度进行检测(图3b)。
2017年,田中克典主任研究员等人开发了从HeLa细胞(人宫颈癌细胞)中识别正常细胞HUVEC(人脐带上皮细胞)的高灵敏细胞识别技术(图3c)。该技术让具备某种反应性官能团的“强”相互作用配体分子(肽配体)与细胞表面上的受体进行第一次相互作用后(预靶向),再让“弱”相互作用的配体分子(糖链配体)与其他受体进行二次相互作用。选择性结合预靶向官能团的反应性官能团及标记基团与糖链配体结合。进行第二次相互作用时,肽配体与糖链配体结合的点击反应仅在这两种配体分别相互作用的两种受体所在的细胞A表面进行。由此会生成人工糖肽,可以通过糖链配体的标记基团选择性地检测细胞A。
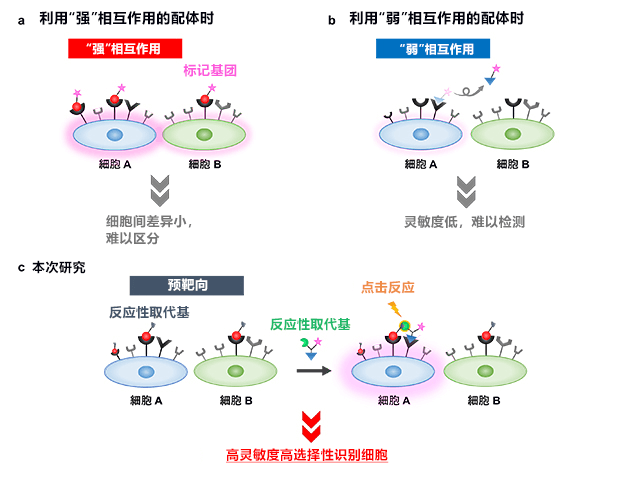
图3:以往的靶细胞识别方法与本次研究开发的方法
a:利用“强”相互作用的配体分子时,即使与细胞A相互作用的受体大量表达,但由于会同时识别细胞A和B二者的受体,所以也很难进行区分。
b:利用“弱”相互作用的配体分子时,即使与受体相互作用也会立即分离,因此无法以高灵敏度进行检测。
c:依次利用“强”相互作用和“弱”相互作用,并通过点击反应使这些配体分子在靶细胞表面结合,可以选择性地识别靶细胞。
研究方法与成果
研究团队为推广先前开发的细胞识别技术,准备了4种“强”相互作用的肽配体和5种“弱”相互作用的糖链配体。然后将其应用于5种癌细胞(HeLaS3:人宫颈癌细胞、A549:人肺泡基底上皮腺癌细胞、BxPC3:人胰腺癌细胞、PC3:人前列腺癌细胞、SW620:人结肠癌细胞)和1种非癌细胞(TIG3:人二倍体成纤维细胞)(图4)。
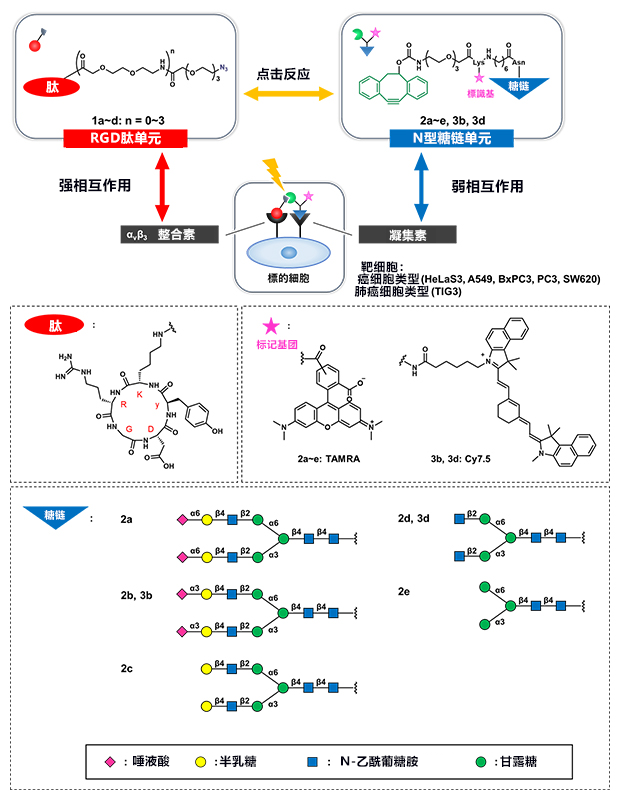
图4:“强”相互作用的肽配体与“弱”相互作用的糖链配体的设计
αvβ3整合素受体的配体分子RGDyK肽单元(1a~1d)、凝集素受体的配体分子N型糖链单元(2a~2e)及标记基团的结构。
采用的6种细胞都表达与RGDyK肽配体“强”相互作用的αvβ3整合素受体。仅通过以前的“强”相互作用识别细胞时,所有细胞都会检测出强烈的荧光信号,无法识别这些细胞(图5右上方的框内)。
而利用此次开发的方法,通过组合“强”相互作用和“弱”相互作用的2种配体,成功对癌细胞和非癌细胞进行了模式识别(图5)。例如,通过为HeLaS3细胞采用末端具有N-乙酰葡糖胺或甘露糖的糖链配体(2d、2e),为A549细胞采用末端具有α(2、3)唾液酸的糖链配体(2b),为BxPC3细胞采用末端具有半乳糖、N-乙酰葡糖胺或甘露糖的糖链配体(2c、2d、2e),成功标记了各细胞。

图5:利用RGDyK肽配体和N型糖链配体选择性标记细胞
如a~f各细胞的右上方框内所示,仅利用以往的“强”相互作用配体无法识别细胞。而利用预靶向法,可通过组合特定配体获得的荧光信号模式来识别细胞。
此外,研究团队还将该方法应用于体内癌组织识别。针对种植性转移了HeLaS3细胞(人宫颈癌细胞)或A549细胞(人肺泡基底上皮腺癌细胞)的小鼠,首先注射“强”相互作用的RGDyK肽配体(1d)进行预靶向,30分钟后再注射“弱”相互作用的糖链配体(3b或3d)标记癌组织(图6a)。此时,标记基团使用可通过近红外线进行标记的Cy7.5。最终,源自HeLaS3细胞的癌组织利用糖链配体(3d),源自A549细胞的癌组织利用糖链配体(3b)检测到了强烈的荧光信号,成功地选择性识别了癌组织(图6b、c)。
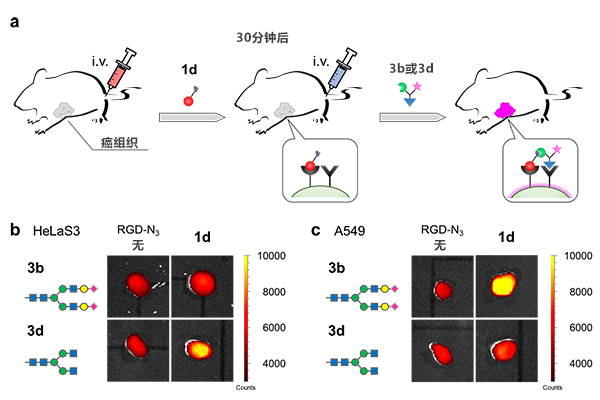
图6:利用预靶向法在体内标记癌组织
a:体内识别的概要。为种植性转移了人类癌细胞的小鼠注射RGDyK配体(1d)进行预靶向,30分钟后再注射糖链配体(3b或3d)。
b:在HeLaS3细胞(人宫颈癌细胞)中,通过组合1d和3d,选择性地识别了癌组织。
c:在A549细胞(人肺泡基底上皮腺癌细胞)中,通过组合1d和3b,选择性地识别了癌组织。
本研究利用在靶细胞上合成的人工糖肽成功对细胞进行了模式识别。经验证,这种模式可用于体内成像,识别特定的癌组织。利用组合这两种2种配体分子识别靶细胞上的多种受体的技术,有望开发出可以选择性识别体内的癌组织和疾病部位的新诊断方法。
论文信息
题目:Cancer discrimination by on-cell N-glycan ligation
期刊:《Communications Chemistry》
DOI:10.1038/s42004-020-0270-9
文:JST客观日本编辑部














