生物药品等领域需求不断高涨的特殊蛋白质存在着生产成本较高的课题。为改变这种情况,日本产业技术综合研究所生物医学研究部门的研究组长大石勋博士着眼于生产成本比较低的鸡蛋,通过基因编辑技术重组鸡的基因,让鸡产下含有大量特殊蛋白质的“金蛋”,实现了低成本制造特殊蛋白质。

让物价“优等生”生产蛋白质
近年来,以生物药品为中心,蛋白质市场迅速扩大。随着再生医疗的研究越来越活跃,诱导未分化细胞分化的蛋白质的需求也不断高涨,预计今后蛋白质的市场将进一步扩大。
不过,蛋白质的制造技术还存在课题。目前主要采用的方法是把想制造的蛋白质的基因导入培养细胞进行生产,但建设和运营制造工厂等需要巨额资金,而且制造重组蛋白质涉及各种专利,甚至被称为“专利丛林”,需要支付大量的专利使用费。
所以,这类特殊蛋白质的制造成本最低也高达每克数千日元,还有不少超过10万日元的,制造成本阻碍了市场的扩大。为此业界尝试通过操作动植物的基因而非培养细胞来生成有用蛋白质,一些技术已经实用化,比如山羊奶和草莓果实等。
日本产业技术综合研究所生物医学部门尖端基因组设计研究小组的组长大石勋,正在进行让鸡蛋含有特殊蛋白质的研究。关于使用鸡蛋的理由,大石解释如下。
“鸡蛋的生产原理非常明确,生产成本非常低,被称为‘物价优等生’。一个鸡蛋的蛋清中约含4克蛋白质,因此即使只能置换其中一部分,也能低于现行的成本来生产蛋白质”。
另外,主要由水和蛋白质构成的蛋清还具有杂质少、易于纯化的优点。基于这些特点,国内外的很多研究人员都在开发利用鸡蛋生产特殊有用蛋白质的技术,但迄今为止尚无实用化的先例。大石说:“原因在于难以改变鸡的基因”。
利用基因编辑技术在目标位置导入基因
要想改变动物的基因,需要操作受精后、细胞分裂前的受精卵基因。因为如果能在单细胞阶段导入基因,重组的基因就可以通过之后的细胞分裂遍布到所有细胞中。但鸡的受精发生在输卵管深处,而且卵细胞上附有巨大的蛋黄,因此几乎不可能导入基因(图1)。
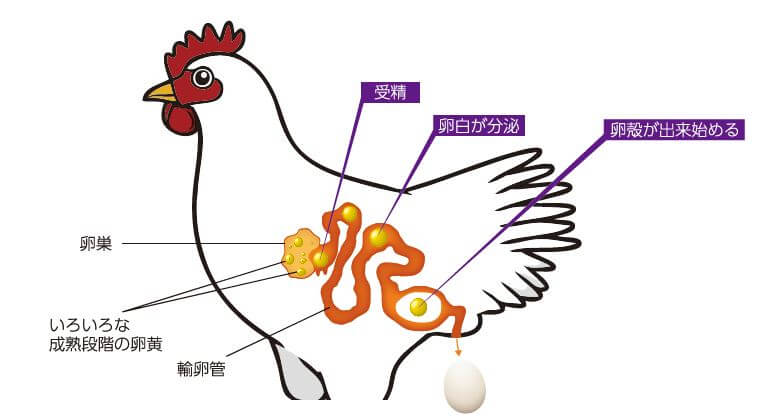
■图1:鸡的受精发生在体内深处,在输卵管内移动24~27小时,期间形成鸡蛋。受精后很难立即取出受精卵,如果是产卵后则细胞增加太多,所以与其他动物相比,基因操作更加困难。
既然无法在受精后立即操作,那么能否向产出的鸡蛋中导入基因呢?于是研究人员又做了另一个实验,即让鸡蛋感染含有目标基因的病毒载体。但难度较大,大石说:“这十几年来,很多研究人员都在挑战这个课题,但存在导入效率低等问题,始终未能从蛋清中获得足够的蛋白质”。
对此,大石尝试的方法是利用从早期鸡胚中提取的原始生殖细胞。原始生殖细胞是成熟后会变成精子和卵子的细胞,如果改变原始生殖细胞的基因并将其移植到其他鸡蛋中,就可以将目标基因导入鸡的体内。
大石回忆说:“这是一家美国的生物初创企业2006年开发的方法。我看了一份报告,里面介绍说通过导入绿色荧光蛋白(GFP)的基因,培育了发绿色光的鸡,我觉得或许可以使用这种方法”。
大石反复进行了实验,但进展并不顺利。促使研究出现转机的,是作为新的基因操作技术开始普及的CRISPR-Cas9基因编辑技术。相对于病毒载体法在染色体哪个位置导入基因完全取决于病毒而言,CRISPR-Cas9则通过将RNA作为向导,能切断目标位置并在该位置导入基因。
为了尽可能多地生产蛋白质,大石确定的导入位置是约占蛋清中蛋白质总量50%的卵清蛋白基因的位置(基因座,图2)。导入的基因选择了干扰素β(IFN-β)。大石介绍说:“(IFN-β)是一种能诱导对病毒产生抗体的生理活性物质,除了用来治疗多发性硬化症、恶性黑色素瘤和肝炎等之外,也作为研究用试剂。目前10微克IFN-β的售价高达2~5万日元,所以极具商业挑战的价值”。

敲开蛋壳上部,在显微镜下注入已导入基因的细胞。把针尖上的细胞注入胚胎,这是一项要求非常精准的工作。
蛋清中含大量IFN-β,通过交配繁殖雌鸡
大石开发的方法是首先从雄鸡的早期胚胎中提取原始生殖细胞,并利用CRISPR-Cas9技术在卵清蛋白的基因座处导入IFN-β基因(图3);然后将该原始生殖细胞移植到其他鸡蛋(受体胚)中后,孵出来的雄鸡就会同时拥有源自转基因的原始生殖细胞的精子和源自受体胚的精子(性腺嵌合体鸡 第0代)。使该雄鸡与未进行基因操作的自然雌鸡交配,孵化出来的就是第一代转基因鸡。第1代转基因雌鸡产的鸡蛋中含有大量IFN-β。
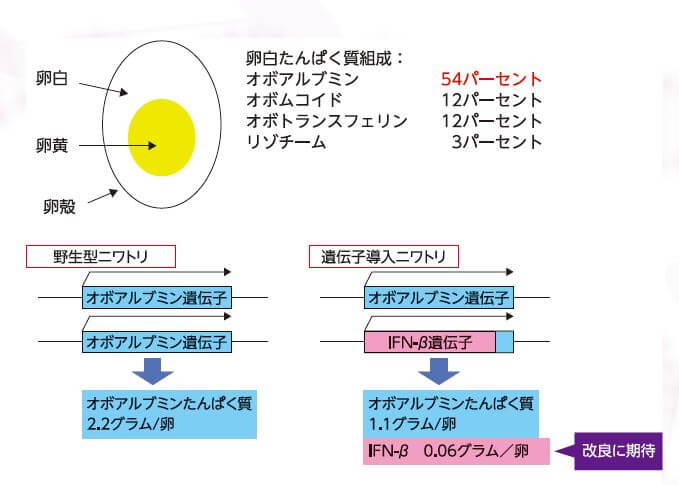
■图2:在蛋清中含量最高的卵清蛋白的基因座中导入IFN-β基因。通过进行基因编辑,可以向卵清蛋白的基因座导入。
大石强调说:“卵清蛋白被认为与蛋壳的形成有关,因此最初一直担心第1代雌鸡能否产蛋。不过最终顺利产蛋,而且每颗鸡蛋含30~60毫克的IFN-β”(图4)。根据IFN-β的售价单纯计算的话,一颗鸡蛋的价格高达6000万日元至3亿日元,真可谓是下“金蛋”的鸡。
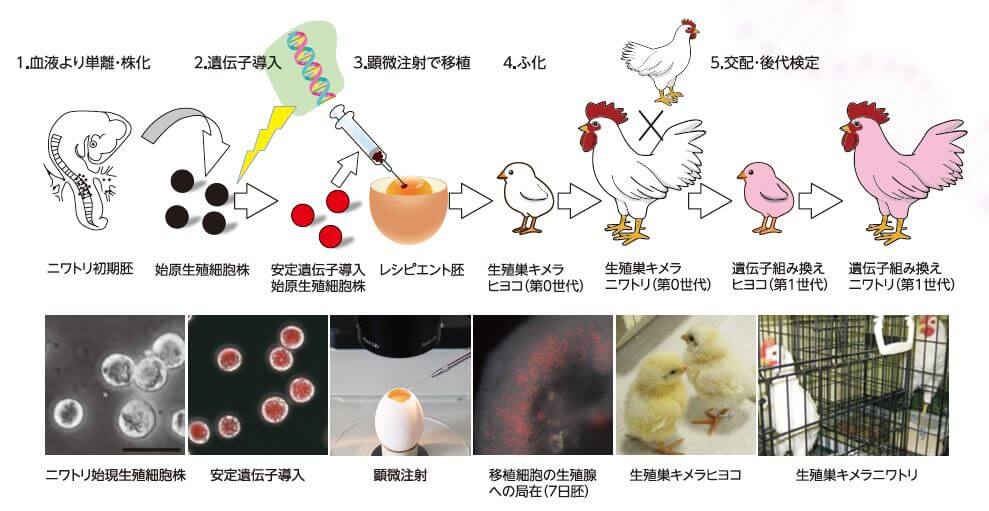
■图3:利用基因编辑技术向鸡体内导入基因。首先提取原始生殖细胞,通过基因操作嵌入目标基因,在显微镜下移植到其他鸡蛋(受体胚)中。使孵出来的雄鸡与未进行基因操作的雌鸡交配,产蛋孵化转基因鸡。
不过,还需要对蛋清进行纯化和实施活性化处理,鸡蛋本身并不能直接卖高价,但利用蛋清生产大量特殊蛋白质的意义非常重大。第1代雌鸡至少能连续产蛋5个月,因此应该可以作为生产有用蛋白质的生物工厂充分进行利用。
大石说:“另外值得一提的是,蛋白质的生产能力还可以通过繁殖传递给下一代”。由于含IFN-β的鸡蛋不能孵化,雌鸡无法留下后代,但让携带IFN-β基因的雄鸡与野生型雌鸡交配就能孵出携带该基因的鸡蛋,然后再孵化出雏鸡(图5)。这样得到的第3代以后的鸡也保留着导入的基因,这表明通过繁殖可以增加下“金蛋”的鸡。大石充满期待地表示:“家禽养殖领域逐渐确立了通过冷冻保存精子将其用于人工授精的技术。如果转基因鸡也能保持精子的话,应该会便于这种方法的推广”。

■图4:含IFN-β的蛋清(左)与普通鸡蛋(右)相比颜色浊白。一颗鸡蛋含30~60毫克IFN-β。
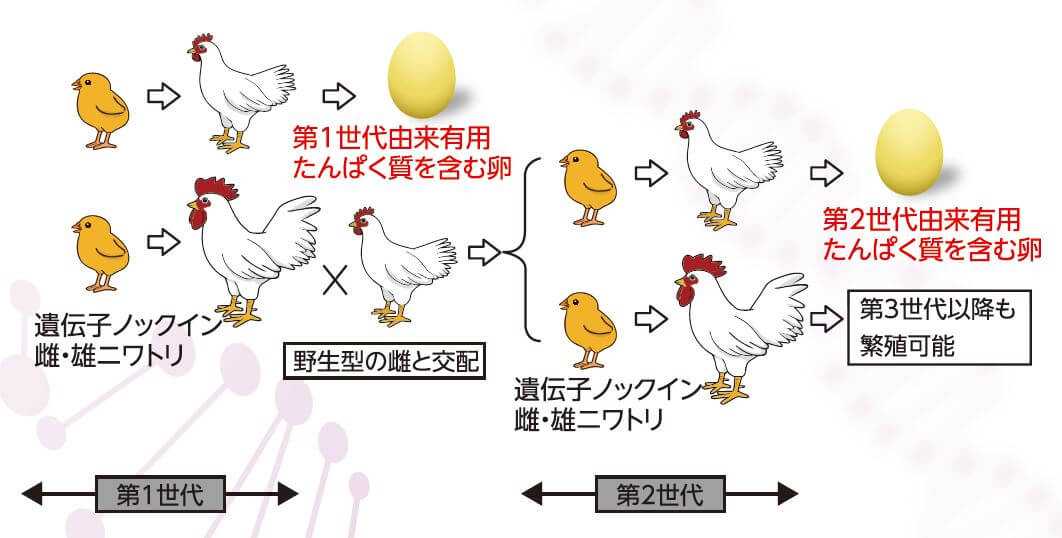
■图5:导入的IFN-β基因可以通过繁殖传递给下一代,因此无需复杂的操作就能繁殖“下金蛋的鸡”。
利用日本企业专利,通过受托生产磨炼技术
利用原始生殖细胞的基因导入法理论上还可应用于IFN-β以外的其他有用蛋白。获得大石的技术授权和经验的Cosmo Bio公司(东京都江东区)已从2019年7月开始受托生产。今后计划推进把企业希望生产的蛋白质基因导入鸡体内,制造和纯化蛋白质的研究开发,目标是通过增加可以应用基因导入法的蛋白质的种类,改良纯化技术。
大石充满信心地表示:“IFN-β虽然取得了成功,但并非所有蛋白质都能一样顺利成功。受基因长度等的影响,也可能无法在蛋清中表达,因此计划积累案例,优化针对各基因的技术非常重要。研究进展顺利的话,有望低成本大量生产各种蛋白质”。
另一方面,推进商业化进程时担心的是用于改变基因的CRISPR-Cas9专利问题。CRISPR-Cas9的专利由海外研究机构持有,用于商业用途的话,需要向持有专利的2家机构支付使用费。因此,大石等人着眼于大阪大学的初创企业C4U(大阪府吹田市)持有专利的CRISPR-Cas3技术。这项基因编辑技术是日本的国产技术,与CRISPR-Cas9专利不冲突,即使支付使用费,也能为振兴国内产业做贡献。
利用鸡蛋生产有用蛋白质的技术正通过与国内企业合作的产官学研合作体制稳步推进实用化。利用国产技术低成本大量生产有用蛋白质的成功,势必会为产业界带来巨大的冲击。

研究室里的带自动转蛋功能的孵蛋机
原文:JSTnews 2019年9月号
翻译·编辑:JST客观日本编辑部














