东京大学药学院有机和药物化学研究室翟璐晗特聘研究员及大和田智彦教授、尾谷优子讲师一起,使用计算化学对被认为与阿尔茨海默氏症(Alzheimer’s Disease, 俗称老年痴呆症)密切相关的β-淀粉样蛋白(Amyloid β,Aβ)的聚集结构进行了拓扑分析(图1),在其疏水核区域首次发现此前从未被科学界关注到的弱电子相互作用,从而揭示了β-淀粉样蛋白沉积的起源[1]。相关研究成果已经发表在2019年7月24日的《Scientific Reports》上[文献1]。
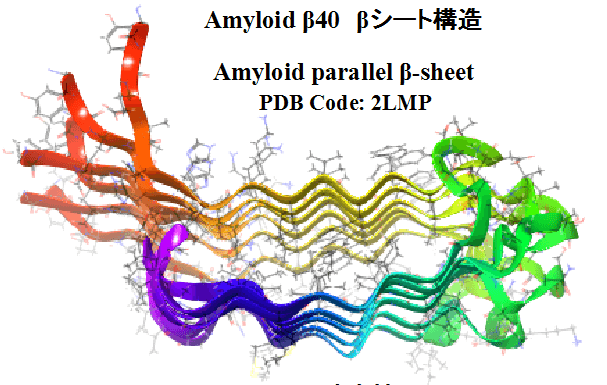
图1 β-淀粉样蛋白40 的β-折叠结构示意
阿尔茨海默氏症最先由德国精神学家与病理学家Alois Alzheimer于1906年发现,是一种发病进程缓慢并随着时间不断恶化的神经退行性疾病,是失智症(痴呆症)的主要大类。2014-2015年间导致美国人十大死因中阿尔茨海默氏症排名第六,但增长趋势远超前五位并是排名第一位心脏病的17倍;在世界卫生组织(WHO)公布的2016年全球前十位死亡原因中位列第五(图2);2017年BBC报道全球前十名死亡原因中失智症(老年痴呆症)位于心血管疾病、癌症、呼吸系统疾病、糖尿病、下呼吸道感染之后,列第六位。目前在发达国家中,阿尔茨海默氏症被认为是耗费最多社会资源的一类疾病。
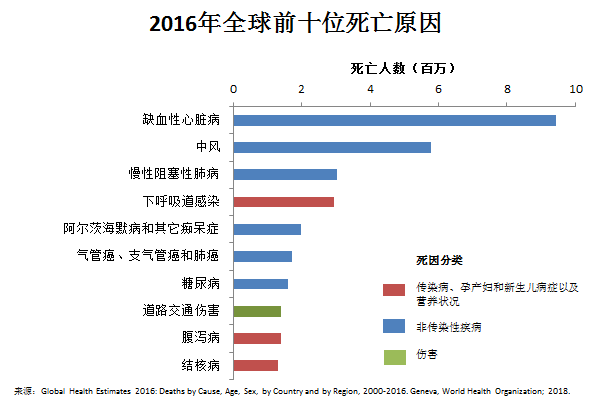
图2 WHO官网公布的2016年全球前十位死亡原因
虽然阿尔茨海默氏症被发现以来已逾百年,但其发病原因至今未有定论。其中占主导的一个推测病因为1991年提出的β-淀粉样蛋白假说。β-淀粉样蛋白是淀粉样前体蛋白( amyloid precursor protein,APP)被蛋白酶水解后产生的约39-43个氨基酸组成的短肽。β-淀粉样蛋白在大脑中聚合堆积形成β-淀粉样斑块(β-amyloid plaques)沉积是阿尔茨海默氏症的主要病理特征之一,并被认为是主要发病原因。也有假说认为未形成斑块沉积的β淀粉样蛋白寡聚体才是致病主谋,这些又被称为淀粉样蛋白衍生可溶性配体(amyloid-derived diffusible ligands, ADDLs),是类似朊病毒蛋白(prion protein, PrP)的一种具有传染性的蛋白质,会引起传递性的神经系统变性病。
β-淀粉样蛋白因含有大量疏水性氨基酸而具备易于聚集堆积的特征,这些聚集形式多是β-折叠(β-sheet)结构(图3)。β-折叠又称β片层结构(β-pleated sheet),属于蛋白质典型的二级结构类型之一。β-折叠中,两条以上氨基酸链(肽链)或同一条肽链之间的不同部分形成平行或反平行排列,一般认为是通过肽链间或肽段间的氢键维系。这每一条肽链或肽段被称为β-折叠股或β-股(β-strand),氢键主要在股间而不是股内。
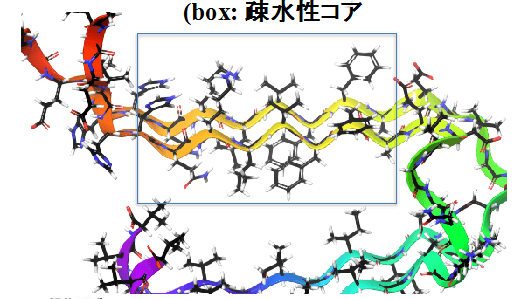
图3 β-淀粉样蛋白疏水性核区域的β-折叠结构
本次研究小组通过QTAIM (Quantum Theory of Atoms in Molecules,分子中的原子量子理论)对β-淀粉样蛋白β-折叠拓扑结构计算分析发现,β-股内空间接近的特定疏水性氨基酸原子间原本微不足道的电子会发生积聚,并最终形成弱电子相互作用;进一步发现,β-淀粉样蛋白的β-股间除了常规的氢键维系外,也由于这些弱电子相互作用的存在而形成更为牢固的网状结构,最终促成β-片层的稳定存在(图4)。
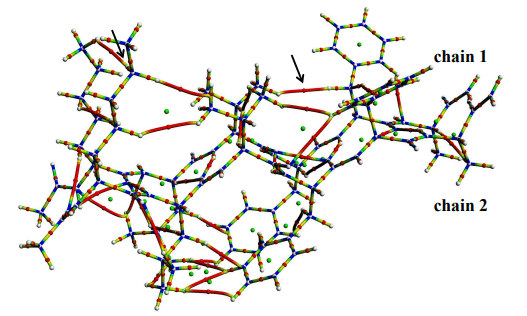
图4 两条β-股间弱电子相互作用示意图
本次发现β-淀粉样蛋白肽链中疏水性氨基酸的侧链之间存在的弱电子相互作用,表明以往所认为的由整体相互作用形成的蛋白间疏水性结构并非均质,而是依存于氨基酸组分中每个原子并且具有明确的方向性。本次对β-淀粉样蛋白聚集结构的微观电子行为分析,揭示了β-折叠及斑块沉积的结构起源,将极大有助于针对阻止β-淀粉样蛋白沉积的新药开发。
供稿 宋傑 东京大学博士
除特别标注外图均取自日文新闻发布稿
编辑修改 JST客观日本编辑部
参考文献:
1.Luhan Zhai, Yuko Otani and Tomohiko Ohwada , "Uncovering the Networks of Topological Neighborhoods in β-Strand and Amyloid β-Sheet Structures," Scientific Reports: 2019.07.24, doi:10.1038/s41598-019-47151-2.
相关链接:
1.东京大学新闻发布稿













