败血症是由体内炎症引起的严重疾病,目前尚无有效的药物能彻底治愈。另外,病情发展速度非常快的恶性脑肿瘤“胶质母细胞瘤(GBM)”会对抗癌药产生耐药性,目前几乎没有有效的治疗药物。治疗这些严重疾病的新药的研发备受期待。
体内发生炎症时,免疫细胞和濒死细胞会释放名为HMGB1(高迁移率族蛋白B1)的核内染色质蛋白。这种HMGB1通过与名为RAGE(晚期糖基化终末产物受体)的特异性细胞膜受体结合,在细胞内引起炎症过程。
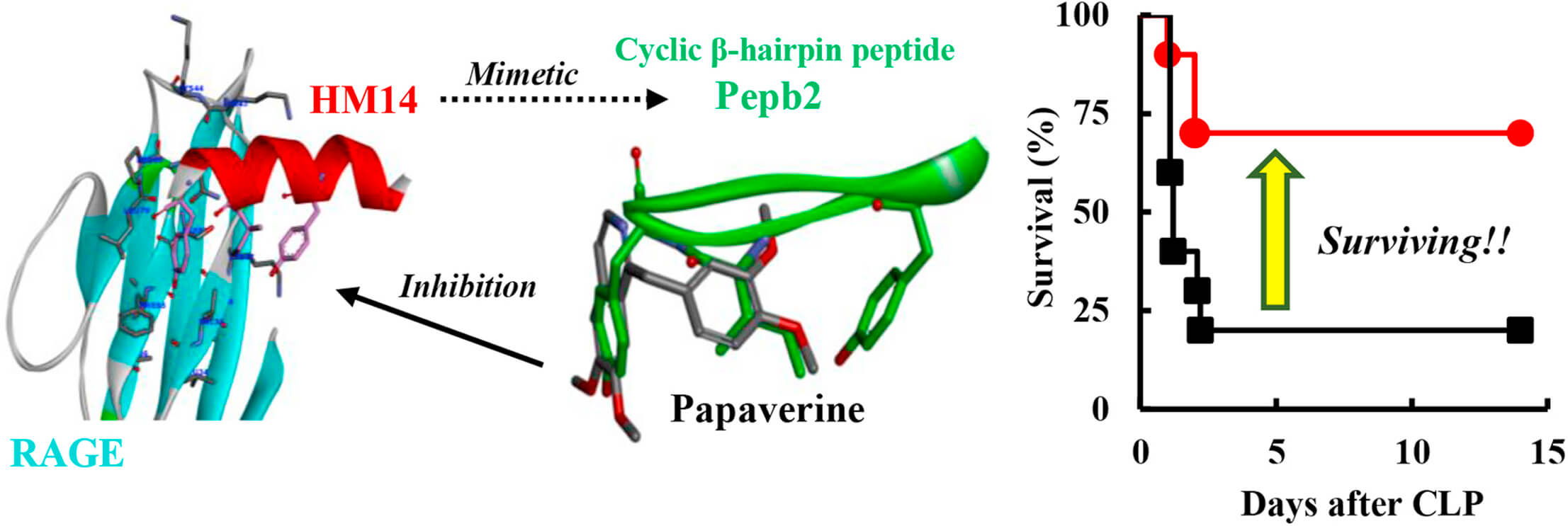
东京理科大学的田沼靖一教授带领的研究小组开发了以蛋白质间的相互作用(PPI)为靶标的计算机模拟(In Silico)新药研发法“COSMOS”,并通过HMGB1与RAGE的结合预测区域对新型环肽进行分子设计,发现其具有RAGE抑制活性。另外,通过进行肽结构相似性解析发现,普通的解痉药“罂粟碱”能抑制HMGB1与RAGE结合,具有抗炎、抗癌等新药效。研究小组利用模型动物进行实验,确认罂粟碱是能够有效治疗败血症和胶质母细胞瘤等的药物。
这种结合计算机技术的新药研发方法和“药物重定位”(Drug Repositioning)方法,有助于在安全性已经得到确认的现有药物中发现尚未知晓的新药效。有关论文已发表于《生物化学与生物物理研究通讯》(Biochemical and Biophysical Research Communications),链接: https://www.sciencedirect.com/science/article/pii/S0006291X19301706?via%3Dihub 。
田沼教授表示:“研究小组通过查明细胞凋亡的控制机制,开发并尝试以蛋白质间的相互作用为靶标的In Silicon新药研发法,制作了细胞凋亡控制化合物。希望制作出用于癌症和阿尔茨海默病等的治疗药物的先导化合物。”
研究重点
利用In Silicon新药研发法发现,1848年发现的传统血管扩张药及解痉药“罂粟碱”,具有抗炎和抗癌作用等。
研究发现,罂粟碱通过抑制受损细胞和免疫细胞释放出来的信号分子(HMGB1)与控制炎症反应的细胞膜受体蛋白(RAGE)结合,来抑制炎症反应,有望用来治疗败血症、癌症(胶质母细胞瘤)、阿尔茨海默病和糖尿病等由身体炎症引起的多种疾病。
利用这种方法进行“药物重定位”,与开发全新的药物相比,在时间、成本和安全性方面效率更高,可以扩大现有药物的治疗范围,以及引领新药开发。
(日文新闻发布全文)
文:JST客观日本编辑部翻译整理














