日本北海道大学研究生院药学研究院的市川聪教授与美国杜克大学的Seok-Yong Lee副教授等人组成的联合研究小组,全面解析了对耐药菌也有效的天然有机化合物与靶酶的复合体结构。
用于治疗细菌感染的抗生素迄今为止挽救了无数生命。不过,使用抗生素会出现对抗生素产生耐受力的耐药菌,因此新药开发的历史可以说是药物与耐药菌之间的“道高一尺魔高一丈”。耐药菌的传播已经成为全球性的严重问题,当务之急是开发对耐药菌也有效的抗生素,这是抵抗耐药菌的“最后堡垒”。
在对抗耐药菌的新型抗生素开发中,与细菌细胞壁的主要成分肽聚糖的生物合成有关的酶MraY受到了关注,目前已经从自然界中分离出了几种能强力抑制MraY的天然有机化合物。
此次,市川教授等人组成的联合研究小组对化学合成的天然产物衍生物群与MraY结合形成的复合体进行三维结构解析,由此提出了“条码系统”,能为抑制MraY的化合物提供合乎逻辑和常理的设计指南。这样就可以根据复合体结构进行药物设计,有望开发出能对抗耐药菌的抗生素,作为抑制耐药菌的“最后堡垒”。
相关研究成果已发布在2019年7月2日(周二)公开的《自然-通讯》(Nature Communications)杂志上。
【研究背景】
已知细菌细胞壁的主要成分肽聚糖是开发抗生素的优良靶标,此前已经开发出了青霉素等β-内酰胺类抗生素和万古霉素等。但现在又出现了对这些抗生素产生耐受力的耐药菌,成为了严重的世界性问题,在全球有数百万人因为耐药菌而死亡。为对抗耐药菌,当务之急是开发具有新的作用机制的抗生素。近年来,合成肽聚糖前驱体——脂质I(Lipid I)的酶MraY(所有细菌生长必不可少的酶)作为开发抗生素的新靶标备受期待。
目前已经从自然界中分离出几种能强力抑制MraY的天然有机化合物。这些化合物的尿苷部分拥有相同的结构,其他结构则有较大差异。
此前一直不清楚这些化合物是如何与MraY相互作用的,以及今后该如何进行分子转换才能进一步“发挥药效”。
【研究方法】
为分析此前化学合成的3种抑制MraY的天然有机化合物(或其衍生物)是如何抑制MraY的,研究小组对复合体结构进行了综合解析。虽然难以对跨膜酶MraY进行X射线晶体结构解析,但此前市川教授等人组成的联合研究小组全球首次对Muraymycin D2(MRY D2)与源自嗜热菌Aquifex aeolicus的MraY形成的复合体成功地进行了X射线晶体结构解析(Nature 2016, 533, 557)。此次试着在相同的条件下获得其他复合体的晶体,但很遗憾未能实现。
因此,联合研究小组向大羊驼(Llama、Lama、Glama)施用MraYAA,通过对生成的多种MraY的单链抗体(纳米抗体)进行解析,获得了约60种纳米抗体。利用其中3种适合结晶的纳米抗体,成功与3种抑制MraY的天然有机化合物进行了共结晶,并对获得的晶体实施了X射线晶体结构解析(图1左)。
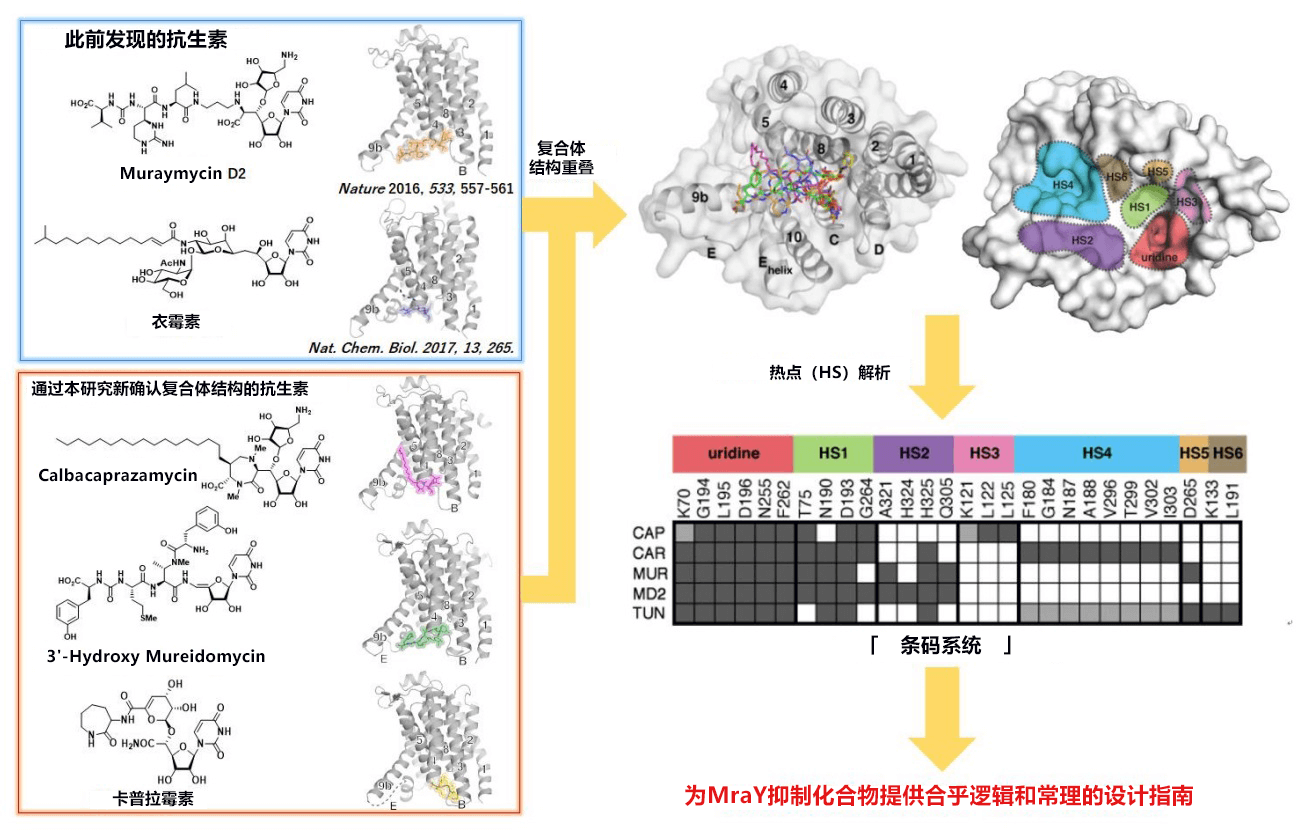
图1.
(左)对成功实现共结晶的MraY抑制天然有机化合物晶体进行X射线晶体结构解析的结果。
(右)可以为MraY抑制化合物提供合乎逻辑和常理的设计指南的“条码系统”。
【研究成果】
通过结构解析发现,所有化合物共同存在的尿苷部均与同一个结合口袋结合,但其他位点形成了不同的相互作用。联合研究小组将这些特征位点分别定义为热点(HS),把尿苷周围、TM9b /Loop E、己内酰胺结合、疎水性、Mg2+结合及衣霉素结合口袋分别命名为HS1-HS6。另外,通过分析化合物与包含6个HS在内的残基形成的相互作用,提出了能为MraY抑制化合物提供合乎逻辑和常理的设计指南的“条码系统”(图1右)。
分析发现,除了与HS1结合外,各种抑制剂必须与至少2个HS相互作用。例如,虽然卡普拉霉素(Capuramycin)属于例外,与HS1及HS3进行结合,但衣霉素与HS4和HS5结合,并在其他化合物不具备的HS6中形成氢键,表明衣霉素拥有与其他化合物不同的HS结合谱。
联合研究小组通过对抑制MraY的天然有机化合物全面实施结构解析,首次发现了以上现象。
【未来展望】
通过利用为MraY抑制化合物提供合乎逻辑和常理的设计指南的“条码系统”,可以根据复合体结构实施药物设计,有望开发出新的抗生素,作为对抗耐药菌的“最后堡垒”。
(日文新闻发布全文)
文:JST客观日本编辑部翻译整理














