日本名古屋大学的研发小组与台湾中央研究院和日本鸟取大学合作,共同查明了不同糖链控制神经轴突生长的分子机制。尤其是名为硫酸软骨素(CS)的糖链,在发生脊髓损伤等外伤或脑梗塞等供血不足时,CS会在受损的轴突尖端诱导出名为Dystrophic endball(营养不良的端球)的异常球状结构,并阻碍受损的神经轴突再生,这是全球首次在分子和细胞水平查明这种机制。
称为神经细胞轴突的部位在人体内发挥着“输电线”的作用,通过电信号传递各种信息。输电线有时会被“台风”等刮断,神经轴突也一样,有时会因外伤等断裂。断裂了的输电线能立即重新接上,但神经轴突无法二次再生。因为CS经由神经细胞受体PTPRσ,将原本具备再生能力的轴突变成了名为Dystrophic endball的异常球状结构,此部分为阻断了其再生能力。
本次研究发现,PTPRσ会使名为Cortactin的分子去磷化,并抑制自噬流动,这是形成Dystrophic endball的主要原因。
相关研究成果已于2019年5月6日发布在英国科学期刊《自然-化学生物学》(Nature Chemical Biology)的网络版上。
人类的神经回路连接成直线的话长达50万公里,形成神经回路的就是神经细胞的轴突。
神经回路很容易因外伤等断裂,比如脊髓损伤等。断裂后神经细胞最远的尖端会发生沃勒变性,但较近的尖端(细胞体侧)仍然存活,因此神经轴突会尝试重新向远端延伸。但中枢神经系统的神经轴突会强力阻止这种再生(图1)。
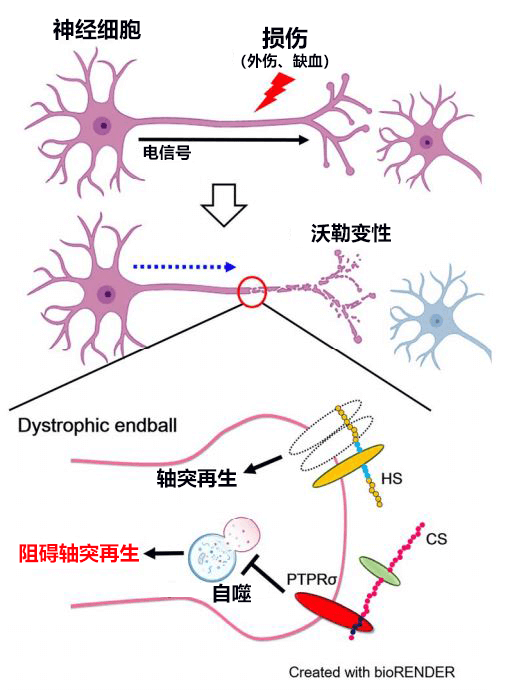
图1:阻碍神经轴突再生
这样神经回路就会被永久切断,导致患者出现麻痹等后遗症。罪魁祸首就是名为硫酸软骨素(CS)的糖链。
因为CS会与神经细胞受体PTPRδ结合,在神经尖端部分诱导名为Dystrophic endball的异常球状结构。另一方面,名为硫酸乙酰肝素(HS)的糖链负责轴突生长,奇妙的是,CS与HS的结构非常相似,都会与同一个受体PTPRδ结合。不过,长期以来一直不清楚这两种十分相似的糖链是如何发挥完全相反的作用的。
研发小组首先化学合成了结构和长度各不相同的一系列HS和CS。对其进行解析发现,HS能够与大量PTPRδ同时结合,因此该受体为多聚体,而CS只能与一个或极少量的PTPRδ同时结合,因此受体为单体。PTPRδ的这种状态差异向神经细胞发送了完全相反的命令。
研发小组还发现,CS会提高PTPRδ的酶活性,使细胞内的Cortactin分子去磷酸化。而磷酸化的Cortactin是完成自噬必不可少的分子。因此,轴突内的自噬被中断,由此抑制轴突生长,在轴突末端形成球状物Dystrophic endball,这是受损轴突的特征之一。
该发现的重要之处在于,查清了通过CS-PTPRδ-cortactin-autophagy这一路径阻碍轴突生长的机制。由此明确了有效治疗神经损伤的靶向分子。例如,HS寡糖和PTPRδ抑制剂等有望成为候选药物。另一个重点是,该发现还有望用来查明帕金森病和阿尔茨海默病等神经退行性疾病的发病机制。因为在这些疾病中也经常发现自噬中断的现象。(日文发布全文)
文:JST客观日本编辑部














