日本横滨市立大学的研究小组通过与日本国立传染病研究所、德岛大学、京都大学和爱媛大学等开展联合研究,明确了引发艾滋病的人类免疫缺陷病毒是如何逃脱宿主细胞防御系统的分子机制。
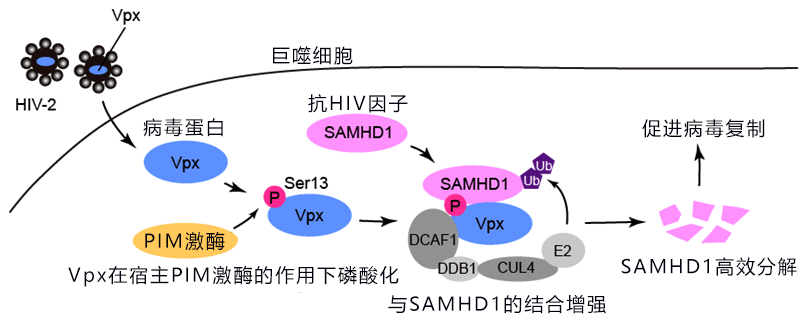
(图):HIV-2蛋白Vpx在PIM激酶的作用下磷酸化,细胞内的抗HIV因子SAMHD1由此被高速分解破坏。
研究背景
HIV(人类免疫缺陷病毒)侵入人体后,会逐渐破坏免疫细胞,导致人类会感染平时不会感染的病原体,从而患上各种疾病。这种状态被称为艾滋(AIDS,获得性免疫缺陷综合征)。据推测,全球目前有3670多万人感染HIV病毒,目前尚无有效的治疗方法能将感染的病毒彻底从体内排除,HIV感染者需要每天坚持服用抗病毒药物。另外,还有很多出现耐药病毒的病例报告,因病毒基因发生突变,现有药物失去了效果。因此,需要开发能预防感染的HIV疫苗,并不断针对现有药物已经不起作用的耐性病毒开发新药。
人体细胞对病毒有着各种防御手段。例如,SAMHD1蛋白是人体细胞产生的一种酶,能强力阻断巨噬细胞和CD4阳性T细胞感染HIV。而HIV病毒、尤其是西非地区感染者较多的HIV-2病毒,其病毒颗粒中含有Vpx蛋白,这种蛋白会在细胞内分解SAMHD1。由此,HIV-2便能感染骨髓细胞和T细胞。研究小组在开发新型抗HIV药物的过程中,想到了抑制Vpx蛋白的功能。由于病毒蛋白质大多都是借助人体细胞内的“病毒调节因子”发挥作用的,因此研究小组首先研究抑制Vpx分解SAMHD1的因子。
研究内容
通过以往的研究人们已经知道,Vpx在细胞内会受到磷酸化修饰,因此研究小组认为,这种磷酸化修饰可能会抑制Vpx对SAMHD1发挥作用。于是便从参与磷酸化修饰的400多种宿主蛋白群中,寻找与Vpx相互作用的物质,最终发现名为PIM激酶的宿主蛋白会与Vpx充分结合,特异性发生磷酸化。研究小组利用质谱仪进行详细调查后确认,Vpx的第13个氨基酸——丝氨酸会在PIM激酶的作用下发生磷酸化。将这种丝氨酸换成其他氨基酸后,Vpx不再发生磷酸化,病毒繁殖显著减少。另外通过基于分子动力学的结构模拟预测,这种丝氨酸的磷酸化会加强与SAMHD1的相互作用,生物化学实验也验证了这一点。
接下来,研究小组利用siRNA使抑制了PIM激酶表达的细胞感染HIV-2,发现这样可大大抑制病毒感染。该细胞中虽然存在Vpx,但细胞内的SAMHD1几乎没有分解,由此可以判断SAMHD1的抗病毒活性得到了保持。
研发小组将现有的PIM抑制剂之一AZD1208注入感染HIV-2的巨噬细胞,发现可长时间抑制病毒的繁殖。因此确认,AZD1208这种现有的抗癌药还具备抑制HIV蛋白Vpx发挥功能的作用,表明了通过药物重定位实现新型抗病毒剂的可能性。
本次研究确认,宿主PIM激酶是抑制Vpx对SAMHD1发挥作用的病毒调节因子。另外还首次证明,通过抑制PIM激酶,可以有效阻断HIV-2的复制。
未来展望
由于对维持HIV-2感染至关重要的病毒调节因子是一种名为PIM激酶的酶,如果以这种酶而不是容易发生突变的病毒蛋白为靶点,就有望开发出不易产生耐药性的新型艾滋病治疗方法。PIM激酶的靶点、即Vpx的第13个氨基酸——丝氨酸会在病毒进化过程中被保存下来,预计该部位的磷酸化是Vpx发挥功能必不可少的区域。因此,只要使用PIM抑制剂等阻断该部位发生磷酸化,应该就能抑制现存所有HIV-2病毒的繁殖。今后,研究小组计划利用现有的PIM抑制剂等进行动物实验等,同时探索模拟Vpx磷酸化区域的肽和化合物等,从而开发以病毒–宿主之间的相互作用为靶点的新型治疗药物。(日文发布全文)
文:JST客观日本编辑部














