
吉森 保
大阪大学 研究生院医学系研究科/生命机能研究科 教授
2017年入选CREST研究代表
证明自噬是哺乳动物的共同机制
引发研究热潮
随着自噬研究不断发现相关的基因簇和机制,开始有越来越多的声音期待将其应用于各种疾病的治疗。尝试将自噬的基础研究成果投入实用化的,正是大阪大学研究生院医学系研究科/生命机能研究科的吉森保教授。吉森目前还在CREST“起因于细胞外颗粒的生命现象阐明及对其进行控制的基础技术开发”研究领域的“基于自噬的细胞外颗粒响应及形成”研究中担任研究代表。
吉森从研究生时代就开始研究以哺乳动物的细胞为对象的细胞生物学,他是受到东京工业大学的大隅良典特任教授邀请才开始研究自噬的。吉森回忆说:“当时大隅博士在自然科学研究机构基础生物学研究所成立了研究室,邀请我做副教授。我当时马上就要30岁了,正在寻找可以作为毕生事业的研究课题。听完大隅博士的介绍后,直觉告诉我,这是一份值得做的工作。”
当时,大隅博士刚刚在酵母中发现了14种与自噬有关的基因,整个领域还没有那么热门。但他确信这种现象是生物的基本功能,于是邀请正在研究哺乳动物细胞的吉森加入。这样研究对象就从酵母扩大到了哺乳动物中。他的决定非常正确,2000年吉森在哺乳动物中也发现了与自噬有关的蛋白质,并证明自噬的基本机制是所有真核生物共有的细胞内净化回收系统。
吉森发现的是相当于酵母的Atg8蛋白的自噬体膜结合蛋白LC3。另外还发现,LC3会被其他自噬相关的蛋白质组脂质化,可以稳定存在于自噬体中。如今LC3已被全球广泛用作自噬的检测标志物,为自噬研究的崛起创造了机会。
识别并消除有害物质
与免疫也有关联
证明自噬能消灭病原菌也是吉森取得的重要成果之一(图1)。在此之前,虽然知道处于饥饿状态时自噬为确保营养会分解蛋白质,但根据吉森的发现明确了自噬与免疫也有关。进一步的研究表明,不仅是细菌,自噬还会选择性消除各种对细胞有害的物质。
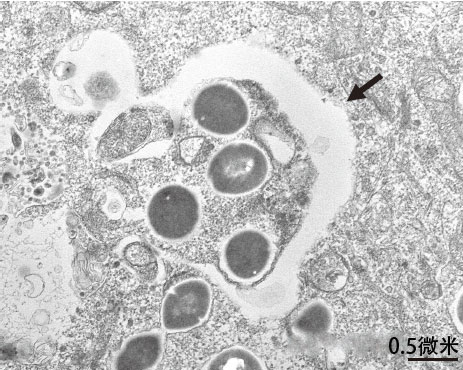
图1:捕获侵入细胞的A组链球菌的自噬体电子显微镜照片
一般来说,从细胞外部进入内部的物质会被名为内体的细胞器吸收并筛选。病原菌也会被内体吸收,但它们会试图刺破内体膜逃到细胞质中,或者通过在内体内开孔来输送自己的蛋白质。吉森仔细观察这种情况发现,包裹细菌的内体膜受损后会发生名为泛素化的蛋白质修饰,启动自噬所需的Atg蛋白由此聚集起来。
根据这个结果,吉森开始认为自噬可能并不会识别和消除病原菌,而是一种为消除受损的内体而发生的现象。他认为,如果这个假设是正确的,那么还可以解释自噬为何能消除表面结构各异的各种病原菌。
吉森利用内体打孔的人造珠子验证了这个假设,果然发生了自噬,人造珠子被自噬体捕获。由此明确了自噬是如何选择各种分解对象的。
从意外的结果到新发现
修复损伤的新途径
接下来,吉森开始调查与内体一样也属于细胞器之一的溶酶体的修复机制。他认为,如果假设正确,其修复过程将以与内体相同的机制进行。溶酶体负责细胞内外成分的分解,囊泡内部为酸性,含有各种水解酶。进行自噬时会用自噬体包裹要分解的物质,并将其移送到溶酶体中进行分解。
当溶酶体受损时,酸性内容物会泄露到细胞质中,引起炎症和氧化应激,甚至细胞死亡。例如,肾脏中堆积的草酸钙晶体会损伤肾小管细胞中的溶酶体,导致结晶性肾病的病情恶化。吉森实际观察受损溶酶体修复的样子发现,像预期那样发生泛素化,而自噬则选择性地对其进行了隔离和修复。
然而,通过进一步分析获得了新的发现。本来应该存在于自噬体中的脂质化LC3还出现在了受损的溶酶体中。详细调查这个意料之外的结果发现,LC3与在溶酶体膜上控制钙出入的钙通道相互作用,促使钙流出。控制基因表达的转录因子TFEB由此被激活,促进了修复(图2)。
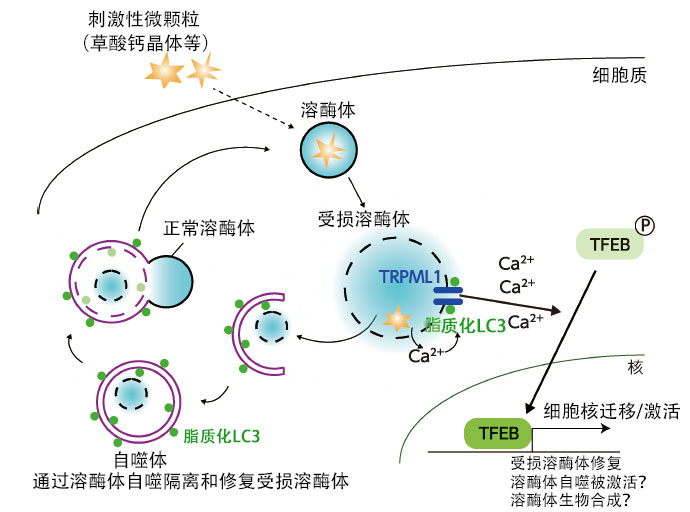
图2:溶酶体受损时,脂质化LC3与溶酶体上的钙通道TRPML1相互作用,促进钙从溶酶体流出。由此会激活转录因子TFEB(负责激活与溶酶体的生物合成和自噬有关的蛋白质的基因表达),促进了溶酶体的修复。
由此确认LC3独立于自噬的溶酶体修复功能发挥作用,并获得了超出吉森预期的结果。他说:“假设被证明是正确的当然很开心,但发现意料之外的现象更令人兴奋。此次也得到了非常有趣的结果。”
吉森抑制患结晶性肾病的模型小鼠的TFEB发挥作用后还确认,与普通的结晶性肾病模型小鼠相比,受损溶酶体增多,肾病恶化(图3)。今后如果能开发出作用于参与溶酶体修复的两种途径的化合物,那么不仅是结晶性肾病,还有望治疗与溶酶体损伤有关的各种疾病。
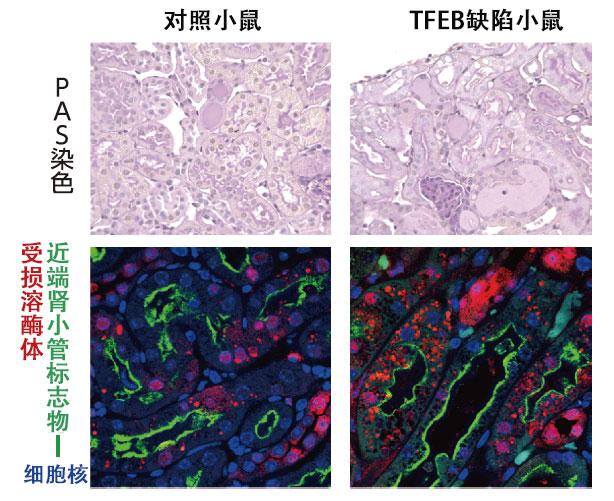
图3:TFEB的功能是预防结晶性肾病恶化。结晶性肾病(草酸钙肾病)模型小鼠的肾组织图像(上)和肾组织免疫染色图像(下)。在TFEB缺陷小鼠的肾脏中观察到更多的受损溶酶体(右下、红色),肾病恶化(右上)。(红色:受损溶酶体,绿色:近端肾小管标志物,蓝色:细胞核)
与医学部成立研究中心
研究自噬与疾病发病的关系
吉森还取得了其他重要成果。即发现了抑制自噬的分子“Rubicon”。Rubicon是抑制与溶酶体融合(自噬的最终阶段)的蛋白质。到目前为止,我们一直试图促进自噬,但如果能控制发挥制动器作用的Rubicon,或许有助于推进药品开发。吉森就这项重要成果表示:“如果能减少Rubicon,自噬将更加活跃地发生。有望开发相关疾病的治疗药物,应该还有助于延长健康寿命。”
事实上,近些年已通过研究证明,Rubicon会随着年龄的增长而增加;当Rubicon被抑制时,线虫和果蝇的自噬功能被激活,致使寿命延长(图4)。另外还发现,抑制了Rubicon的小鼠,即使投喂高脂肪食物,肝脏中的脂肪堆积和由此引发的肝损伤也会受到抑制,由此Rubicon受到的期待和关注不断升高(图5)。
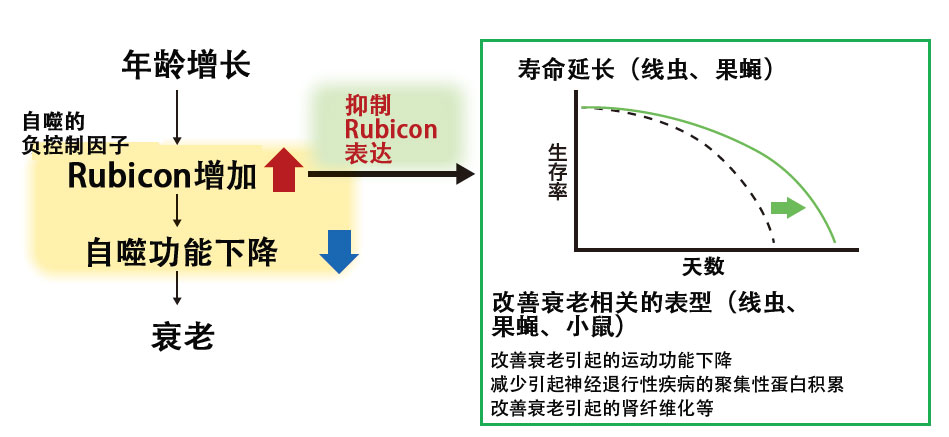
图4:自噬功能随着年龄的增长而降低的机制。随着年龄的增长,Rubicon会增加,导致自噬功能下降,发生衰老现象。抑制Rubicon的表达,可以延长寿命并改善衰老导致的运动功能下降等,观察到与衰老相关的表型改善。
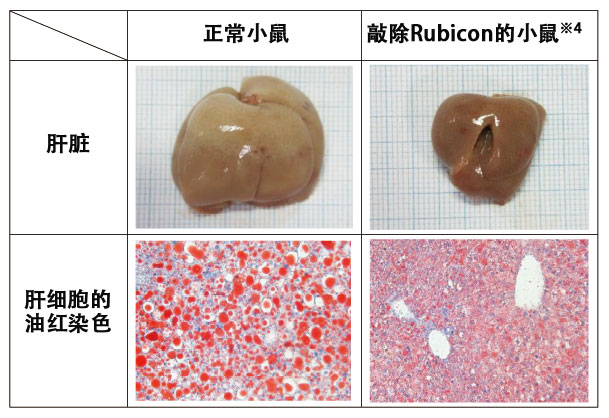
图5:高脂肪饮食小鼠的肝脏及肝细胞比较。抑制Rubicon的表达后,因高营养饮食而肥大的肝脏恢复正常大小,抑制了细胞内的脂肪(下图,红色)积累。
为这种推进医疗应用的研究提供支持的,是2015年成立的大阪大学医学部附属自噬中心。吉森正与专门研究各种疾病的医学部临床教室开展联合研究。他高兴地说:“医学部的教授们也认为一些疾病可能与自噬有关。自噬中心的建立使联合研究变得更加方便,并取得新的成果。”
另一方面,并非所有与自噬有关的生命现象都已被阐明,还有很多人仍在等待治疗药物。基础研究的重要性仍未改变,但已经明确的成果必须尽快通过临床进行验证。吉森就今后的构想表示:“今后的研究将不会过度偏重基础研究或应用研究的某一方,而是应该像车的双轮那样齐头并进。”
建立一个研究生态系统
验证效果推出值得信赖的产品
不仅仅是上述事例,自噬研究的应用范围正在大幅扩大(图6)。吉森为响应这些社会期待,尽快将研究成果回报给社会,于2019年成立了大阪大学校办初创企业“AutoPhagyGo”(图7)。他作为该公司的技术顾问支持研发,2020年7月推出了第一款商品——与UHA味觉糖公司共同开发的有助于健康长寿的营养食品“自噬习惯”。可以说迅速实现了研究成果的实用化。
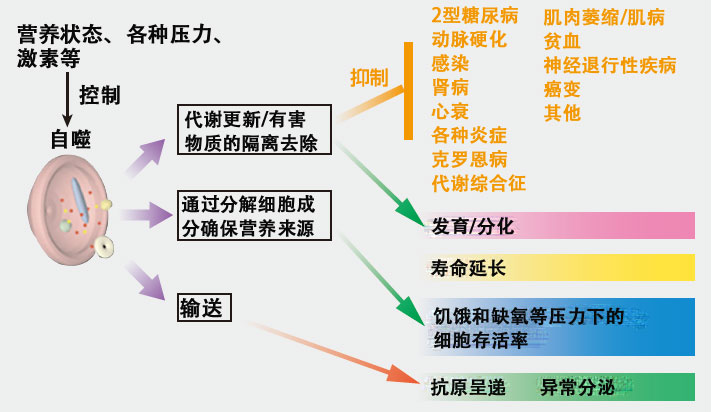
图6:自噬的主要功能

图7:AutoPhagyGo的业务模式
为了实现健康长寿的社会,不仅是食品,AutoPhagyGo还在以化妆品和膳食补充剂等为中心,与多家企业推进联合研究。但是,吉森的目标不仅仅是实用化。他表示:“AutoPhagyGo的目标是通过与多家企业推进联合研究,将实用化获得的利润用作接下来的研究经费,建立研究一个生态系统。”投资也仅限于赞同这种理念的机构和个人。
到目前为止,大学等的研究都是利用以JST为首的公共研究支援机构提供的研究经费开展的。然而,随着研究经费的逐年消减,许多研究人员发现在不稳定的雇佣制度下,每天都在为新的申请书而烦恼。吉森就成立初创企业的原因表示:“为了继续产生好的成果,在稳定的环境中静下心来开展研究非常重要。因此,我们希望建立一个能从民营企业募集研究经费,也可以将研究获得的利润用作研究经费的体制,所以选择了初创企业这种形式。”
为建立这种机制,还成立了一般社团法人日本自噬联盟。与吉森等众多学术界的研究人员一起,AutoPhagyGo和各行各业的著名企业等16家企业作为企业会员加入了该联盟。在这里可以共享最前沿的研究成果,并向公众传播基于科学的准确信息,目标是让整个行业赢得信任。吉森表示:“为了获得信任,充分进行效果验证非常重要。全行业将相互学习最新的研究成果,并开发衡量效果的技术。”
自1992年大隅博士发现自噬以来已经过去30年。我们现在终于可以享受其中的部分成果了。但是,这也是一个至今仍存在未知领域的深奥世界。令吉森等众多研究人员着迷的自噬世界今后会取得什么样的成果呢,让我们拭目以待吧。
文:JSTnews 11月号
翻译编辑:JST客观日本编辑部
【相关阅读】
【自噬开创的新世界】(一)60年研究历程,现状与未来
【自噬开创的新世界】(二)阐明蛋白质的结构,“液-液相分离”是反应的关键
【人物】跨越生物化学和细胞生物学的科学家——水岛升(上)
【人物】跨越生物化学和细胞生物学的科学家——水岛升(下)














