以胰腺癌、胆管癌等为代表的难治性癌症的特征之一是在被称为“间质”的癌细胞以外的区域,会出现数量超过癌细胞的癌症相关成纤维细胞(cancer-associated fibroblast:CAF)的反应性增生。在这类癌症中,可观察到CAF围绕癌细胞巢增生的表现。CAF是一类在胶原蛋白等细胞外基质的产生方面能力出众的细胞,这些细胞外基质的沉积会诱导间质纤维化。已知纤维化引发的癌组织硬化会激活癌细胞,提升其增殖能力及侵袭能力。此外,还已知癌组织的纤维化及硬化会诱导肿瘤血管塌陷、缺血性微环境形成、药物递送效率下降以及免疫抑制性微环境的形成。

图1 名古屋大学研究生院医学系研究科的榎本笃教授(供图:名古屋大学)
尽管过去此前曾尝试开发抑制CAF增生、或是杀伤CAF的治疗方法,但临床试验及临床研究均未取得成功,因此杀伤及抑制CAF的战略已到了重新审视的时期。我们转变以往思路,旨在开发出一种新型治疗方法,以自主鉴定的CAF标志物分子为靶点的抗体药物偶联物(antibody-drug conjugates:ADC)向胰腺癌细胞高效递送抗癌药物。
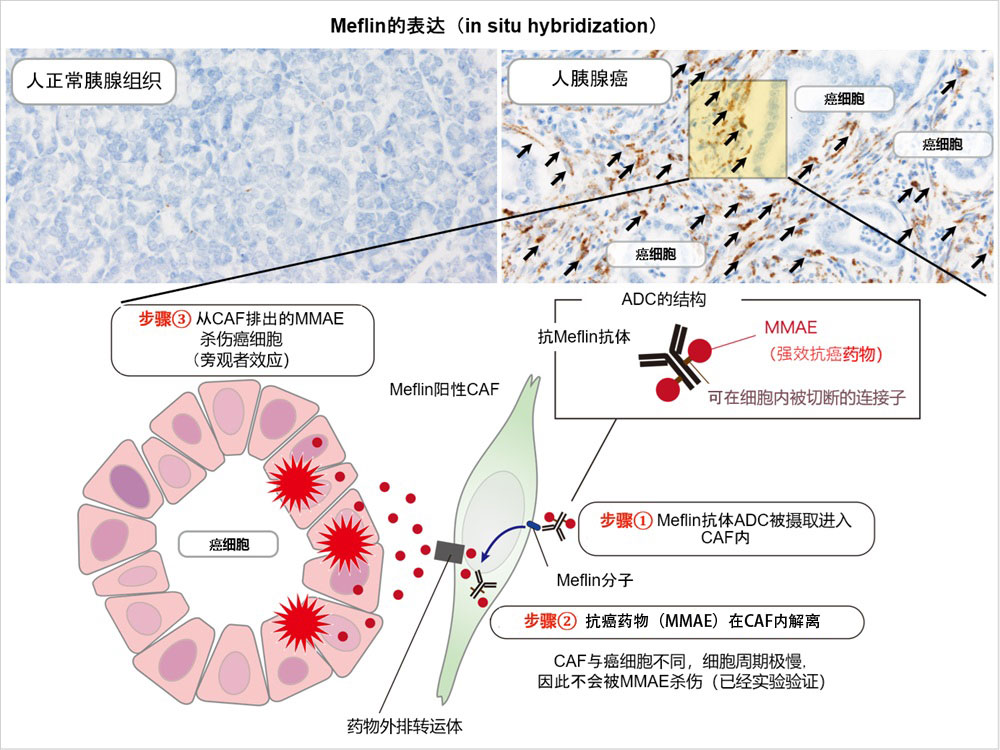
图2 Meflin在人胰腺癌CAF中的表达及抗Meflin-ADC的药效机制(供图:名古屋大学)
本图模式化地展示了本次研究课题旨在开发的抗Meflin-ADC的药效机制。抗Meflin-ADC被Meflin阳性CAF摄取后,在CAF内释放的有效载荷被排出至细胞外,进而杀伤周围的癌细胞(旁观者效应)。
我们于2019年,将胞外结构域带有富亮氨酸重复序列的GPI锚定型分子Meflin,鉴定为CAF最具特异性的膜分子标志物。通过基因修饰小鼠、自发性癌症小鼠模型、人类病理组织样本等开展的验证,已逐步阐明Meflin阳性CAF极敏锐地聚集于癌细胞周围,在转移灶的CAF中也有表达,且与其他CAF膜标志物分子相比,显示出较高的mRNA表达水平。除胰腺癌外,我们已确认该分子在胆管癌、大肠癌、肺癌、乳腺癌、尿路上皮癌、肾癌等多种伴随间质纤维化反应的癌症中,均特异性表达于CAF。同时我们也证实,Meflin虽在正常组织的间质细胞中也有表达,但其表达水平远低于CAF。
迄今为止,我们已获得多株抗Meflin单克隆抗体,并制备了通过连接子在这些抗体上偶联有效载荷的ADC(以下简称抗Meflin-ADC)。截至目前,我们已在多个荷瘤小鼠模型中发现,抗Meflin-ADC具有显著的抗肿瘤效果。
我们预期,抗Meflin-ADC的药效机制,是ADC被摄取进入CAF细胞后,经蛋白酶从ADC上释放的有效载荷通过药物外排转运体被排出至细胞外、进而杀伤邻近癌细胞的“旁观者(Bystander)效应”。此时CAF不会被杀伤,这一点已在采用培养细胞的实验体系中得到确认。
基于上述验证结果,我们设定的目标为:验证抗Meflin-ADC疗法相较于现有细胞毒性抗癌药物的优势,以及旁观者效应的详细药理机制;开展采用GMP级ADC的安全性试验,以及启动针对不可切除进展期胰腺癌患者的I期临床试验。
现已证实,Meflin阳性CAF在绝大多数伴随间质纤维化反应的癌症中均可观察到。此外,与伴随抗癌治疗的选择压力或病程进展,不断获得治疗耐药性或积累基因突变的癌细胞不同,已知CAF的表型十分稳定。我们期待未来有一天,抗Meflin-ADC能够广泛应用于上述多种癌症,或是已对其他治疗药物产生耐药性的癌症。
原文:《科学新闻》
翻译:JST客观日本编辑部