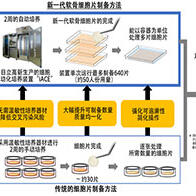
日本厚生劳动省于2026年3月6日有条件并附期限地对两款使用人工多能性干细胞(iPS细胞)的再生医疗产品发放了生产销售许可。这两款产品分别面向重症心力衰竭和帕金森病患者,是全球首次获批的“日本产”iPS细胞治疗产品。预计这两款产品最早将在年内应用于临床。
iPS细胞是通过向皮肤等体细胞人工导入数种基因,使其获得分化为人体的多种细胞和组织的细胞。自2006年京都大学的山中伸弥教授等人宣布在小鼠中成功制备出该细胞以来,已过去了约20年。日本率先使再生医疗成为常规疗法,除此次实现临床应用的疾病外,针对其他疾病的临床试验也在推进之中。对患者而言这意味着治疗选择的增加,同时也提升了人们对新型疗法问世的期待。
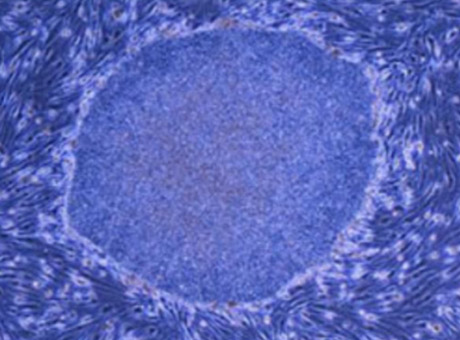
iPS细胞的显微镜图像(山中伸弥/京都大学及日本科学技术振兴机构提供)
大学初创企业与研发型企业推动产品开发
日本厚生劳动省下属的专家委员会于2月19日同意在满足特定条件且设定期限的前提下同意两项产品用于临床,之后厚生劳动省正式批准了这两款产品的上市。获批产品包括:由大阪大学衍生的初创企业“CUORiPS”(东京)开发的“ReHeart”,以及住友化学集团旗下研发型制药企业“住友制药”(大阪市)开发的“Amchepry”。
“ReHeart”主要用于治疗因冠状动脉狭窄或闭塞导致心肌缺血、心功能下降的“缺血性心肌病”所引发的重症心力衰竭。其原理是将来自他人iPS细胞培养得到的心肌细胞制成片状,贴附于心脏表面,使其定植并促进其形成新的血管。在临床试验中,该产品已为8名患者实施移植,所有患者的症状均有所缓解,心功能等指标也出现了改善。
“Amchepry”则用于治疗帕金森病。该病由大脑中分泌神经递质多巴胺的神经细胞减少所引发。治疗方法同样利用他人iPS细胞,诱导其分化为多巴胺神经前体细胞后,移植至患者脑部。在临床试验中共有7人接受移植,其中6人确认能够产生多巴胺。
鉴于两款产品的临床试验样本数量较少,日本厚生劳动省专家委员会依据“若能确认安全性并可推定有效性的前提下,则可设定附带条件及期限,予以提前批准”的制度,做出了批准的决定。条件是在最长7年的批准期限内,通过实际临床使用进一步确认其有效性,确认有效后,可转为无条件许可。
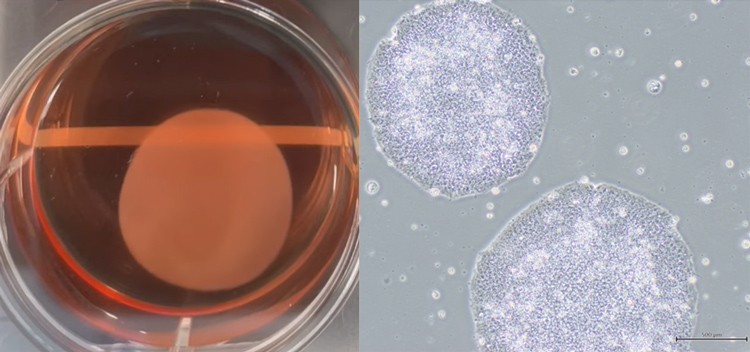
源自iPS细胞的心肌片(左图,摘自CUORiPS的介绍视频)与住友制药培养的iPS细胞(右图,由住友制药提供)
多方科研努力跨越难关实现应用
凭借荣获2012年诺贝尔生理学或医学奖的山中教授的划时代研究成果,再生医疗产品得以在全球首次实现实用化,而这背后,离不开研究和相关开发人员为克服诸多难题所付出的非同寻常的努力。
关于利用iPS细胞的再生医疗,虽然从一开始就备受期待,但也有人指出其安全性方面的隐患。其中最具代表性的就是源自体细胞的组织可能发生癌变。在移植组织时,如果残留了未分化的iPS细胞,就存在癌变的风险。虽然移植的细胞来自患者自身,不易发生排异反应,但仍需谨慎确认是否确实没有发生排异反应。
针对癌变风险,日本厚生劳动省的研究团队于2016年对iPS细胞基因组进行分析,并提出若发现了可能与致癌相关的基因突变,应避免进行移植。针对这些担忧和课题,以山中教授所属的京都大学iPS细胞研究所(CiRA)为首,日本国内许多大学和研究机构的研究人员持续开展研究并取得了诸多成果。
2014年,日本国立研究开发法人理化学研究所(简称,理研)等机构首次成功实施了将利用iPS细胞制备的视网膜细胞移植至患者体内的手术。此后,大阪大学和庆应义塾大学率先开展心脏疾病应用研究。2016年,信州大学等团队宣布,通过将细胞移植至患有心梗的模型猴体内,成功恢复了其心功能。
另一方面,在2016年,北海道大学与庆应义塾大学的研究团队宣布,利用不易患癌的裸鼹鼠,解析了抑制iPS细胞癌变的基因作用机制。2017年,京都大学又开发出可去除具有癌变风险细胞的方法。为实现“安全再生医疗的实用化”的目标,日本各大学和研究机构之间都在不断加强合作。
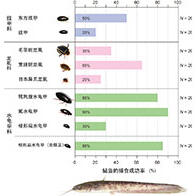
即使移植到活体中也不会形成肿瘤的裸鼹鼠的iPS细胞(北海道大学等提供)
糖尿病、脊髓损伤、癌症之后的新挑战
在多家研究机构稳步推进再生医疗实用化研究的背景下,CUORiPS于2025年4月、住友制药于同年8月分别向日本厚生劳动省提交了上述两款产品的生产销售申请。
这两款产品率先提交了申请并最终获得批准,同时还有其他多种疾病的再生医疗研究同样在稳步推进之中。
据日本厚生劳动省等机构介绍,目前以获得再生医疗产品销售许可为目标的临床试验及临床研究正在多个领域展开,包括:加龄性黄斑变性(理研等)、1型糖尿病(京都大学)、再生障碍性贫血(京都大学)、外伤性脊髓损伤(庆应大学)、角膜上皮干细胞缺损症(大阪大学等)。
此外,iPS细胞在癌症治疗领域的应用也备受期待。日本千叶大学附属医院与理研于今年1月宣布,利用iPS细胞制备出攻击癌细胞的“自然杀伤T(NKT)细胞”,并在针对头颈部癌症患者的临床试验中,8名患者中有2人获得了肿瘤缩小的效果。此外,针对卵巢癌(CiRA与国立癌症研究中心东医院)等多个癌症的治疗研究也在进行中。

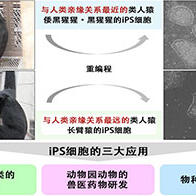
利用iPS細胞制备NKT细胞,然后应用于头颈部癌症患者的流程图(千叶大学病院/理化学研究所提供)
山中教授:“审慎的同时稳步推进”
日本厚生劳动大臣上野贤一郎在6日内阁会议后的记者会上谈及此次批准的意义时表示“希望不仅能为日本,也能为全世界患者带来福音”。不过,此次的批准毕竟还是附带条件及期限的批准,需要在规定时间内收集更多数据,最终证明其疗效,才能取得“正式批准”。

内阁会议后的记者会上的厚生劳动大臣上野贤一郎(3月6日、厚生劳动省提供)
今后,为了使利用iPS细胞制作的医药品能在更广泛的医疗领域得到应用,对前两例的安全性和疗效进行严谨的验证工作必不可少。目前担任CiRA名誉所长的山中教授在厚生劳动省专家委员会批准该申请时发表了如下评论。
“在小鼠iPS细胞相关论文发表20周年的重要节点,能够朝着社会应用迈出重要一步,我感到非常高兴。然而,要将其确立为一种医疗手段,还需要通过更多病例验证其安全性和有效性。我认为,重要的是不急不躁、科学上保持审慎态度,继续一步一个脚印地稳步前进。”

在名古屋市某酒店进行演讲的山中伸弥教授(2016年1月、笔者拍摄)
原文:内城喜贵/科学记者 JST Science Portal 编辑部
翻译:JST客观日本编辑部
【相关链接】
厚生劳动省《上野大臣记者会见概要(2026年3月6日)》
文部科学省《关于使用iPS细胞的全球首个再生医疗等产品获批“大臣谈话”》
CUORiPS株式会社官网
CUORiPS《关于取得人类(同种)iPS细胞来源心肌细胞片附条件及附期限制造销售批准》
住友制药《关于在日本取得非自体iPS细胞来源多巴胺神经前体细胞“Amsheplie”的制造销售批准的通知》