在当前的癌症治疗领域,采用小分子化合物或抗体药物的分子靶向药物,因对特定靶标因子具有高亲和性,已成为治疗的主流手段。但这些传统疗法大半以“单一基因(或蛋白质)”为靶点,在多条信号转导通路失调、且由异质性细胞群形成的癌症中,无法获得充分治疗效果的情况屡有发生。

图1 广岛大学研究生院医系科学研究科高桥陵宇副教授(供图:广岛大学)
此外,传统癌症治疗还存在两大壁垒。第一,存在大量基因虽与癌症的恶性进展及转移密切相关,但由于受蛋白质结构问题(Undruggable target)的限制,现有分子靶向药物难以对其进行调控;第二,对单一分子的抑制会引发代偿性信号激活,最终导致肿瘤获得“耐药性”,这会严重恶化患者的预后。社会各界迫切期待创制出可攻克上述难题的新型治疗模式。
为打破这一现状,我们将目光投向了作为新一代抗癌药物的核酸药物,尤其是非翻译型RNA的一种——微RNA(microRNA:miRNA)。miRNA具有现有药物不具备的的“多分子靶向能力”,能以单个分子对带有互补序列的多个靶信使RNA(mRNA)的表达进行广谱性抑制。
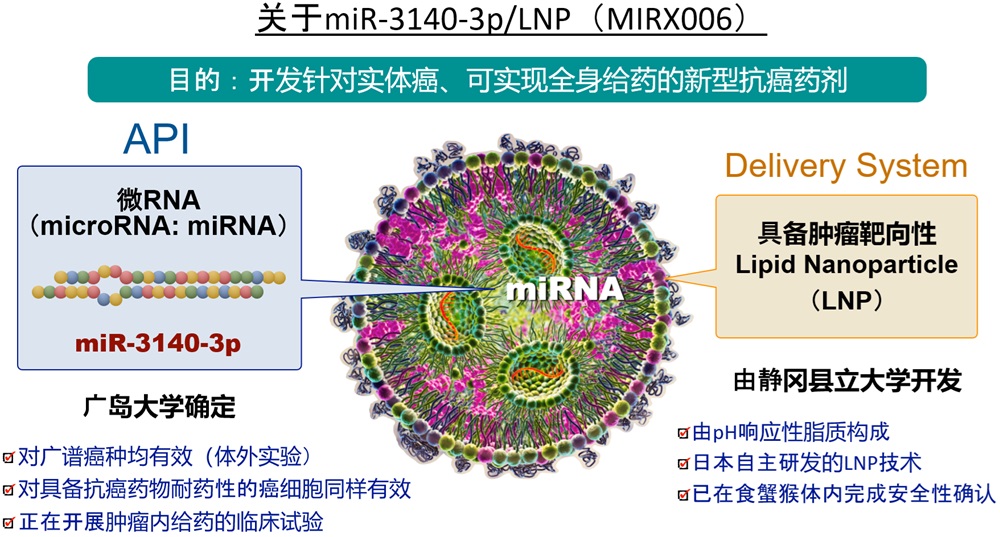
图2 miR-3140-3p/LNP制剂(MIRX006)的开发(供图:广岛大学)
研究团队在既往研究中已独立发现特定miRNA“miR-3140-3p”具有极强的抗肿瘤效果。对于癌症这类同时存在多种基因异常或复杂信号调控紊乱的疾病,可全面靶向多条信号通路的miR-3140-3p,有望成为极有效的新药研发种子。本研究将miR-3140-3p作为核酸药物的主要成分,旨在实现传统分子靶向药物无法达成的“杜绝耐药性的癌症治疗”。
核酸药物实现实用化的最大壁垒,在于向靶组织的递送效率、生物体内的稳定性,以及避免对正常组织产生副作用。本研究为最大限度发挥miR-3140-3p的潜能,正同步开发高度肿瘤选择性递送系统。
具体利用了实体瘤周围微环境相较于正常组织呈“酸性(低pH)”的生理学特征。本研究设计了以仅在特定酸性条件下可被细胞摄取的“pH 响应性脂质”为材料的脂质纳米颗粒(LNP),借此构建了一套可兼顾保持血液中稳定存在、到达肿瘤组织时响应酸性环境并高效释放导入miRNA的递送系统。本技术的目标是,实现即便全身给药也能将副作用降至最低、同时具备极高治疗效果的药物递送。
本研究将具备强效抗肿瘤活性的“miR-3140-3p”与“肿瘤选择性递送技术”相融合,推进了全身给药型新型核酸候选药物“MIRX006”的开发。研发工作将围绕以下两大主轴开展:第一是生物学评价,旨在通过跨癌种的有效性验证、详细作用机制的阐明,以及安全性试验,积累非临床数据;第二是物性方面的相关研究与生产开发,旨在实现脂质纳米颗粒优化,并确立面向药品开发的生产工艺。
通过深化这两大方向的研究,将切实推动MIRX006实现“临床进阶(进入临床试验)”。本研究的完成,不仅将会为难治性癌症患者提供新的治疗选择,也将为日本核酸药物研发技术平台的确立做出重大贡献。
原文:《科学新闻》
翻译:JST客观日本编辑部