日本国立研究开发法人理化学研究所生命医科学研究中心的秦咸阳高级研究员、铃木治和团队总监,以及千叶县癌症中心研究所、岐阜大学、东京慈惠会医科大学的研究团队联合发表研究成果称,发现转录因子之一的MYCN蛋白会促进原发性肝癌的发生。研究团队开发出了一种能够反映MYCN基因表达空间分布的“空间特征评分”,可用于预测肝癌发病风险。通过早期干预,将有望改善肝癌患者的预后并提升其生活质量(QOL)。相关研究成果已发表在《PNAS(美国科学院院刊)》的2月18日刊上。
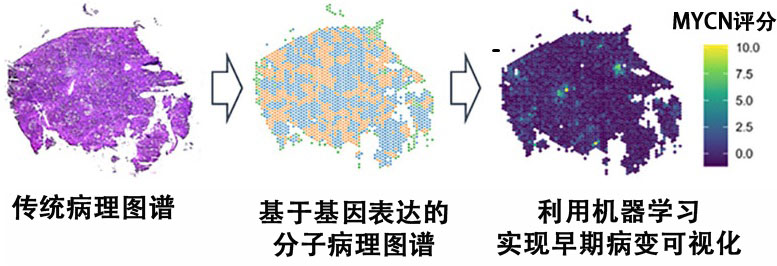
图1 研究概念图(供图:理化学研究所)
2020年全球肝癌死亡人数超过83万人,过去20年间增长了约1倍。据报告,肝癌治疗后5年内的复发率高达79%,因此开发早期发现和预防技术已成为当务之急。
肝脏由肝实质细胞(肝细胞)及其余非实质细胞(免疫细胞、成纤维细胞、血管构成细胞等)构成,这些细胞之间形成了一个相互作用复杂的“微环境”。在慢性肝损伤中,肝细胞的坏死与病理性再生反复发生,导致整个肝脏转变为促进癌症发生的微环境,由此引发多中心性复发,即多个部位发生癌症。
此前,研究团队一直在致力于探索决定非环状类视黄醇抑制肝癌复发反应性的候选因子,并确定了癌基因MYCN是非环状类视黄醇的靶点。此外,还开发了血液中MYCN定量检测方法,并证实血液中MYCN可作为筛选对非环状类视黄醇有反应患者的生物标志物。虽然MYCN基因本身没有突变,MYCN在肝癌干细胞中的特异性表达水平与肝癌的恶性程度相关。另一方面,已知MYCN基因在正常肝脏中的表达水平较低,而在肝脏再生时,特别是在部分切除术后48小时的活跃肝细胞分裂期,其表达会呈现一过性峰值。
因此,本次研究旨在通过阐明肝癌微环境中的MYCN基因动态及其调控机制,验证是否能够区分生理性肝再生与病理性肝癌发生。
首先,研究人员将MYCN基因导入小鼠肝脏,并确认其可促进肝肿瘤的形成。
随后,通过空间转录组学分析,追踪了肝癌模型小鼠肝组织中MYCN基因表达的时空变化,并鉴定出具有肝癌干细胞样特征信号的MYCN高表达区域。
该区域的出现频率随癌变过程增加,且在空间上与肝癌肿瘤标志物Afb的高表达区域相邻。在MYCN微环境中,确认了参与维持癌肝细胞性质的通路的显著激活。周围还观察到了巨噬细胞的聚集。
此外,研究发现炎症性巨噬细胞的培养上清液可在肝细胞中诱导MYCN表达,而肝细胞中MYCN的过度表达则会降低其对巨噬细胞刺激的反应性。这表明MYCN表达与炎症反应之间存在相互影响的反馈调控机制。同时,研究团队还利用机器学习算法开发了“MYCN评分”,用于量化MYCN微环境的空间特征。
将该计算公式应用于人类肝细胞系的基因表达数据库后,发现非肿瘤组织中的MYCN评分与肝癌复发风险存在强相关性。研究表明,若非肿瘤组织中存在类似MYCN的致癌微环境,则未来肝癌复发的可能性较高。
秦高级研究员表示:“包括肝癌在内的上皮性肿瘤的发生,是由微环境中多种因子的复杂相互作用引起的,但其全貌一直难以掌握。本研究通过结合空间组学与机器学习,成功对肝癌微环境的整体状况进行了定量评估。今后,我们将进一步推进空间特征评分作为生物标志物的临床应用,同时阐明机器捕捉到的计算公式所揭示的肝癌发病本质。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Proceedings of the National Academy of Sciences of the United States of America(PNAS)
论文:Oncogenic function and transcriptional dynamics of MYCN in liver tumorigenesi
DOI:10.1073/pnas.2521923123