名古屋大学学术研究与产学官合作推进本部的浜口知成特任讲师、大野钦司名誉教授(现任名古屋学艺大学教授)等组成的研究团队指出难以治疗的慢性特发性便秘是由两种肠道细菌协同作用引发的,并提出了新概念“细菌性便秘”,有望为治疗方法的开发提供方向。相关成果已发表在《Gut Microbes》的2月18日刊上。
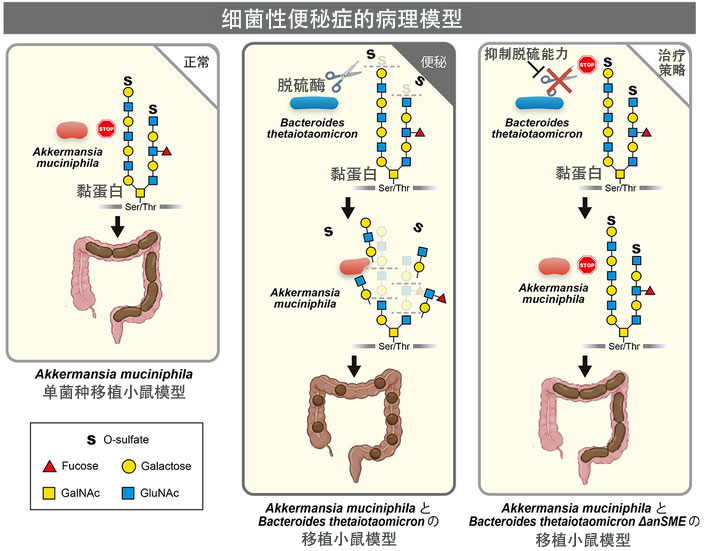
图1 细菌性便秘症的病理模型(供图:名古屋大学)
便秘是以排便次数减少、粪便坚硬为特征的常见消化系统疾病,其病因此前一直被认为是“肠道蠕动功能下降”。然而,对于与肠道蠕动无关、病因不明的慢性特发性便秘症(CIC)以及帕金森病(PD)伴随发生的便秘,其发病机制此前一直不明确。CIC及PD相关便秘难以通过泻药或刺激性药物得到改善。
因此,此次研究团队关注了可保持粪便水分、使肠道内润滑的成分“肠道黏液”,验证了肠道黏液被肠道细菌分解而引发便秘的可能性。
肠道黏液以高分子糖蛋白黏蛋白为主要成分,黏蛋白具有高保湿性,覆盖于肠道内侧,在保护肠壁免受细菌侵害的同时,还承担着使排便顺畅的润滑剂作用。
首先,为确定致病肠道细菌,研究团队对从全国收集的147名健康者、231名帕金森病患者、54名慢性特发性便秘患者的粪便进行了16S解析及qPCR解析。结果发现,患者粪便中B.thetaiotaomicron 和A.muciniphila 两种细菌出现异常增殖。
接下来,为研究这些肠道细菌的功能,研究团队开展了将细菌移植给无菌小鼠的实验。结果显示,单独移植任一细菌均不会引发便秘,而同时移植两种细菌则会出现粪便变硬(重量降低)、排便次数减少的便秘症状。这表明两种细菌协同作用引发了便秘。而移植8种肠道细菌的无菌小鼠(对照组)则未出现便秘。
此外,通过肠壁通透性实验证实,在两种细菌共存的情况下,肠道屏障功能受到抑制,出现肠漏(肠道通透性增加)。
已有报道称,B.thetaiotaomicron 具有脱去硫酸基团的功能,而A.muciniphila 不具备该功能,但能够特异性分解黏蛋白。基于此,研究团队验证了B.thetaiotaomicron 脱去保护黏蛋白的硫酸基团,再由A.muciniphila 对其进行分解的可能性。
研究团队制备了失去肠道黏膜脱硫功能(缺失anSME酶基因)的B.thetaiotaomicron 菌株,并将其与A.muciniphila 共同定植于无菌小鼠体内,结果确认便秘得到缓解。研究还证实,将该菌株与A.muciniphila 同时移植给小鼠后,小鼠的粪便团块数量及粪便重量均有所增加,便秘受到抑制。
浜口特任讲师表示:“我们认为,细菌性便秘症是由于细菌本身分解黏蛋白黏液的能力异常升高而发病。作为治疗思路,目前还只是提案阶段,但可以考虑开发抑制关键开锁酶作用的药物,或使用不感染人体、仅特异性感染并清除细菌的噬菌体进行治疗。今后我们将致力于开发以细菌而非以人体为靶点、副作用更少的根本性治疗方法。”
大野名誉教授表示:“本次我们提出‘细菌性便秘’并阐明其机制,有望实现靶向性更高的治疗。增强酶活性的药物开发难度较高,相比之下,抑制酶活性的药物虽然相关研究较少,但我们认为其实现可行性相对更高。”
注 无菌小鼠:
指在体内及体表完全不存在任何微生物的状态下饲养的小鼠。它们在特殊隔离装置(Isolator)中,被喂食完全灭菌的水和饲料进行培育。本研究中,通过向这些无菌小鼠仅投予特定细菌使其定植,制备了悉生小鼠。另外,开展本研究的实验室首任教授宫川正澄于1954年在世界上首次成功培育出无菌豚鼠。当年宫川教授开创的“无菌动物”研究技术历经数十年,至今仍被应用于医学生物学研究。本研究与发展了无菌动物实验的实中研(CIEM)共同进行,并接受了技术指导。
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Gut microbes
论文:Bacterial constipation: Mucin-degrading intestinal commensal
bacteria cause constipation
DOI:10.1080/19490976.2025.2596809