东京大学研究生院理学系研究科的黑田真也教授、该研究科附属基因实验设施的守田启悟助教等人的研究团队与新潟大学、奈良尖端科学技术大学院大学、九州大学生体防御医学研究所、庆应义塾大学尖端生命科学研究所展开联合研究称,利用小鼠揭示了引发肥胖的病理现象。研究发现,小鼠肝脏的饥饿适应能力在结构上对肥胖具有稳健性,但在时间上却表现出脆弱性。该发现将有助于理解肥胖和糖尿病等的病理机制并促进治疗方法的开发。相关研究成果已发表在国际学术期刊《Science Signaling》的4月22日刊上。
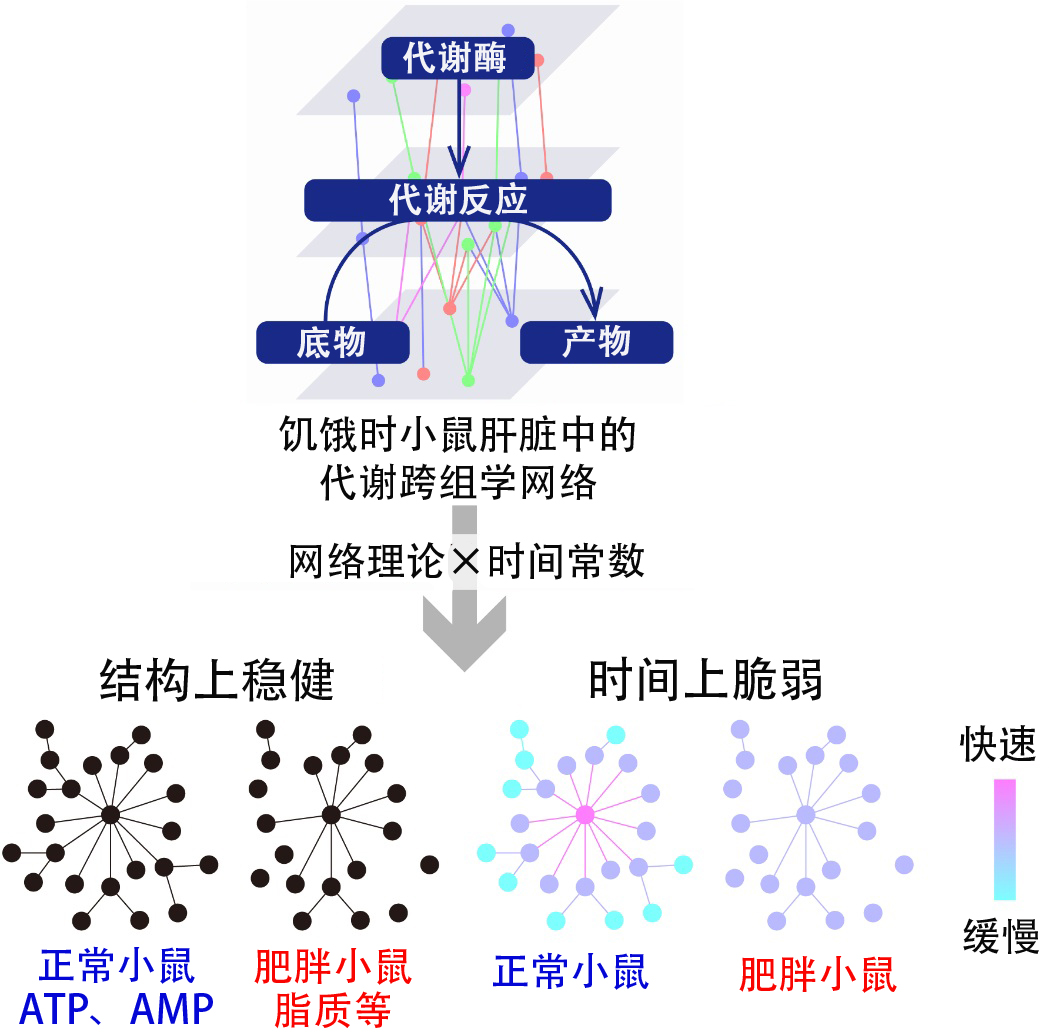
图1:饥饿时小鼠肝脏中的代谢跨组学网络在结构上稳健但在时间上脆弱(供图:东京大学)
饥饿时,生物体需要按时间顺序调动大量分子,以维持进食前的代谢体内平衡。然而,关于实现这些调控的设计原理以及肥胖引起的病理变化,此前并不十分了解。
为此,研究团队聚焦于作为代谢中心的肝脏,对正常小鼠和肥胖模型小鼠(欠缺食欲抑制激素瘦素的小鼠)在饥饿状态下的肝脏进行了水溶性代谢物(糖类和氨基酸等)、脂质、游离脂肪酸/酰基肉碱/酰基辅酶A、转录组、蛋白质和蛋白质磷酸化的全面检测,并提取了显著变化的分子。
研究团队利用数据库确定了所提取分子调控的代谢反应,并通过将它们相互连接,构建了小鼠肝脏在饥饿时的代谢跨组学网络。
此外,为整理难以分析的庞大数据,研究团队采用网络理论和时间常数(响应速度的指标)进行分析,从而对该网络进行了解析。
结果显示,正常小鼠肝脏中形成了以ATP和AMP等能量相关代谢物为中心的无标度样网络(由少数枢纽和大量末端组成的网络)。而在肥胖模型小鼠中,尽管ATP和AMP被脂质等取代,但仍保持了无标度样网络结构。这表明网络结构对肥胖具有稳健性。
另一方面,通过时间常数解析发现,该网络对肥胖表现出脆弱性。在正常肝脏中,ATP及其代谢物AMP等位于网络中心的分子响应更为迅速,使糖原分解、糖异生(由氨基酸等代谢物合成葡萄糖的代谢反应)和脂肪酸分解能够有序地响应。而肥胖模型小鼠则失去了这种秩序,显示出对肥胖的脆弱性。
黑田教授表示:“近年来,生物学领域也能获得大量数据。但是,将这些数据不仅仅是用于单纯的筛选,作为系统来理解也并非易事。此次通过将基础网络理论与生物学相结合,我们成功地从系统层面捕捉到了对生物生存至关重要的饥饿适应机制。”
原文:《科学新闻》
翻译:JST客观日本编辑部
【论文信息】
期刊:Science Signaling
论文:Structural robustness and temporal vulnerability of the starvation-responsive metabolic network in healthy and obese mouse liver
DOI:10.1126/scisignal.ads2547