铃木 勉
东京大学 研究生院工学系研究科 教授
2020年起任ERATO研究总负责人
核糖核酸(RNA)一般被认为是在DNA遗传信息合成蛋白质的过程中起中介作用的分子。但近年来的研究表明,它还直接参与维持生命机能、诱发疾病等多种生命现象。东京大学研究生院工学系研究科的铃木勉教授致力于探究RNA被其他分子附加的“RNA修饰”机制,阐明RNA修饰调控生命机能的原理,并通过调控RNA修饰,为建立服务于新药研发和疾病治疗的技术基础贡献力量。
类似三叶草的结构
单一位点的甲基化引发性质剧变
生物的遗传信息被写入细胞核内的脱氧核糖核酸(DNA)中。DNA信息被转录到信使RNA(mRNA)后输送至细胞核外,之后,核糖体根据mRNA的碱基序列连接氨基酸,合成构成生物体的蛋白质。在这一过程中,转运RNA(tRNA)负责按照遗传信息连接氨基酸(图1-左)。tRNA具有类似三叶草叶片的结构,其上结合着与mRNA的三联碱基序列相对应的氨基酸。
一个分子与糖或甲基等基团结合的现象被称之为“修饰”,在化学领域,这也是制备拥有特定性质分子的常用方法。转录后的RNA在细胞内也会发生同类反应,20世纪后半叶,研究人员发现tRNA能够接受结合甲基的甲基化、结合乙酰基的乙酰化等多种修饰(图1-右),这些被被统称为“RNA修饰”。
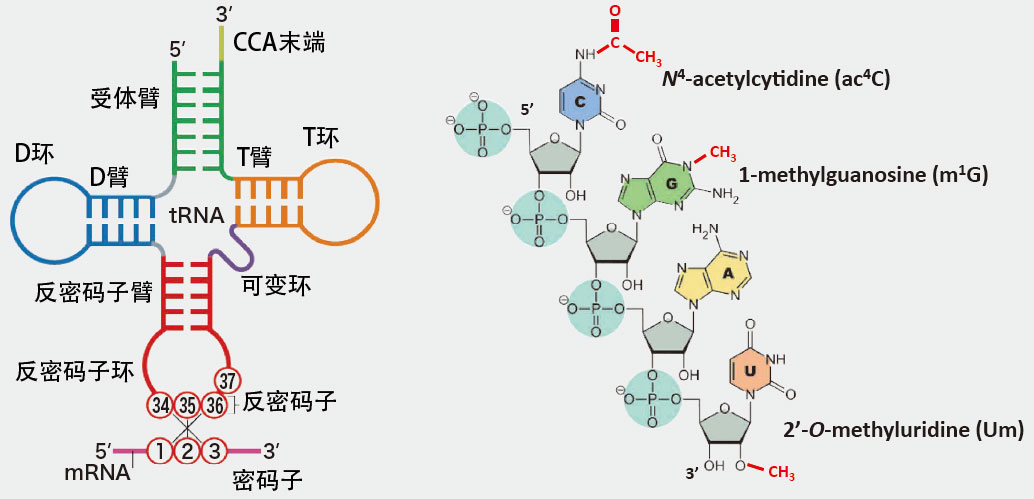
图1 tRNA的结构(左)。tRNA折叠形成L型立体结构,3'末端结合氨基酸,第34、35、36位的反密码子与mRNA上被称为密码子的三联碱基序列互补结合。右图标红部分为RNA修饰的实例。上方两处为碱基发生的修饰,下方一处为核糖发生的修饰。
东京大学的铃木勉教授正是被RNA修饰所吸引的学者之一。约30年前,他还是东京工业大学(现东京科学大学)的学生时,进行tRNA相关研究的他发现tRNA存在大量修饰并深受触动,之后便开始了对RNA修饰的研究。他回忆道:“仅单一位点的甲基化,就能引发性质剧变,这一发现令我十分震惊。”
已发现超150种修饰,新“面孔”不断涌现
2020年开始在ERATO启动研究
与RNA同为核酸分子的DNA也会接受修饰,但人体的DNA修饰几乎仅限于胞嘧啶这种碱基的甲基化,其他类型仅发现数种。与之相比,RNA修饰已发现超过150种,且新的修饰类型还在不断发现之中。在21世纪发现的23种RNA修饰中,铃木教授的研究团队发现了13种,据称还有约20种尚未发表的新发现。
铃木教授作为2020年启动的日本国立研究开发法人科学技术振兴机构(JST)的ERATO“铃木RNA修饰生命机能项目”的研究总负责人,解析DNA遗传信息转录后的基因表达调控机制。为阐明RNA修饰所担负的机能以及与生命现象的普遍性关联,研究团队按照“发现”“解析”“操控”三大方向研究RNA修饰(图2)。项目由4个研究团队构成,不仅探索新型RNA修饰并解析其功能,还开发革新性RNA修饰分析技术与机能操控技术,力求阐明疾病成因以及构筑新药研发和疾病治疗的技术基础。
| 子项目 | 研究概要与目标 |
| “发现” | ⚫解析从包括人类在内的多种生物中分离纯化的RNA分子,探索新型RNA修饰并确定其化学结构。 ⚫运用高灵敏度质谱分析法,鉴定RNA修饰的种类与位点,阐明RNA修饰的机能。 ⚫利用纳米孔测序与深度学习技术,开发单分子水平的RNA修饰定量分析技术。 |
| “解析” | ⚫鉴定RNA修饰酶及其对应基因,阐明RNA修饰的生物合成与机能。 ⚫针对各类RNA修饰酶,构建合成酶基因敲除的小鼠模型,通过小鼠的表型探究RNA修饰的生理功能。 ⚫阐明由RNA修饰异常引发的疾病的发病机制。 |
| “操控” | ⚫通过对RNA修饰酶进行工程化改造,治疗由RNA修饰异常引发的疾病(RNA修饰病)。 ⚫研发RNA修饰酶抑制剂,推动新药研发。 ⚫开发通过照射特定波长红外光激发RNA、从而激活或干扰RNA修饰功能的技术。 |
图2 铃木RNA修饰生命机能项目概要
支撑生物耐热性的“挂锁”
明确可逆性磷酸化修饰
“铃木RNA修饰生命机能项目”目前已发表了超80篇研究论文。2022年发表于《Nature》期刊的《发现支撑生物耐热性的“锁”》是“发现”方向的重要研究成果。该研究在tRNA中发现可逆的磷酸化修饰,并阐明这一修饰能赋予tRNA耐热性和抗RNA降解酶的特性,从而提升生物的耐热能力。
磷酸基结合的磷酸化修饰在蛋白质中十分常见,但在RNA中发现该修饰尚属铃木教授团队首创。铃木教授研究室的大平高之助教在研究耐高温古菌的tRNA时,发现碱基第47位点的尿苷发生了磷酸化修饰(图3-左)。进一步研究发现,无法产生该修饰酶的突变株,在高温环境下的生存率会下降(图3-右)。
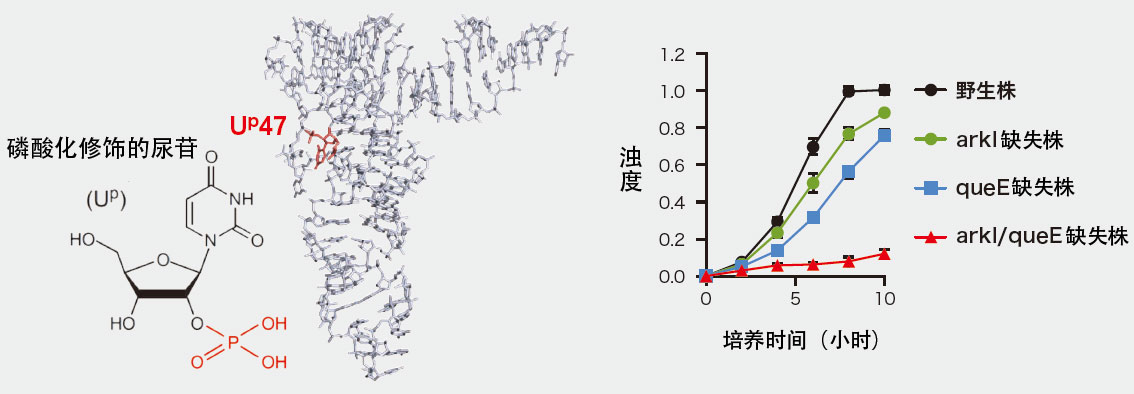
图3 左图为发生磷酸化修饰的尿苷(Up)的结构及其在tRNA中的位点(Up47)。右图为研究87℃条件下古菌耐热性的实验结果。纵轴单位是以波长660纳米(1纳米为十亿分之一米)光测量的浊度。同时缺失产生Up的修饰酶基因(arkI)和赋予tRNA结构刚性的基因(queE)的菌株,在高温下的生存率显著降低。
为阐明这种修饰为何与耐热性有关,铃木教授团队与东京大学研究生院新领域创成科学研究科的富田耕造教授团队合作,进行了X射线晶体结构解析。tRNA折叠形成L型立体结构时,疏水性碱基聚集在内部,使立体结构趋于稳定,但在高温环境下,其立体结构会发生崩溃,由于这种热变性而丧失机能。而磷酸基具有亲水性,它会在立体结构中朝向溶剂侧,即外侧,从而能够有效阻止高温下的结构崩溃,起到稳定结构的作用。
铃木教授比喻道:“这种磷酸化修饰并非将立体结构完全固定,而是在赋予立体结构一定柔韧性的同时防止热变性。就像挂锁一样,允许一定程度的活动余量,同时又能维系住立体结构。”
从菠菜中获得重要成果
发现“环境响应型开关”
2025年,铃木教授的团队发现了一种普遍存在于植物的叶绿体、线粒体,以及霍乱弧菌、绿脓杆菌等部分致病性细菌中的新型tRNA修饰。为了开展研究,团队在学校附近的超市采购了40kg菠菜,并使用自主研发的用于纯化微量tRNA的“全自动往复循环色谱仪”(图4),从菠菜中纯化出了3.3毫克tRNA。

图4 为纯化微量RNA自主研发的全自动往复循环色谱仪系统,从中可见研究团队为推进RNA修饰研究做出的技术创新。
此外,研究团队还证实,此次发现的修饰在蛋白质合成过程中起到了不可或缺的作用。铃木教授笑着说:“有人可能会觉得,40千克材料只能提取3.3毫克的tRNA吗?但其实这种材料利用率已经算好的了。”上述通过调控tRNA功能的重要研究成果,将有助于植物的培育以及对病原菌感染性疾病的治疗。
同年12月,研究团队在全球首次发现,在低氧环境下,大肠杆菌的核糖体RNA(rRNA)中“RNA骨架”会发生甲基化修饰。这种新型的骨架甲基化能微调控核糖体的结构与活性,提高低氧环境下的翻译效率,起到促进生长的“环境响应型开关”作用。该成果揭示了RNA修饰感知生长环境、调控蛋白质合成的全新机制,同时也有望为无细胞蛋白质合成以及合成生物学研究提供重要的技术基础。
鉴定出两种“加糖”的酶
对生物健康成长不可或缺
作为“解析”方向的研究成果之一,铃木教授团队于2023年在《Cell》杂志上发表了“tRNA的糖修饰调控蛋白质合成速度”。该研究鉴定出了两种分别将半乳糖和甘露糖这两种糖添加到tRNA上的酶,并阐明了其分子基础构造。此外,研究还表明,这些修饰能够调控蛋白质合成速度,通过小型热带鱼斑马鱼的实验证实,其对生物的健康成长至关重要。
部分tRNA的第34位碱基发生了特殊修饰,修饰后的碱基还会进一步添加半乳糖或甘露糖。这一现象早在1976年就被发现,但其详细机制和功能此前一直不明。铃木教授研究室的两名研究生分别发现了向该修饰碱基添加半乳糖的酶“QTGAL”和添加甘露糖的酶“QTMAN”,细胞实验证实,若缺乏这些酶,mRNA合成蛋白质的翻译速度会加快,且新生蛋白质无法正确折叠。也就是说,tRNA的糖基化修饰通过调控蛋白质合成速度,维持适当的翻译速度,从而有助于维持蛋白质的质量和机能。
此外,通过斑马鱼实验发现,无法遗传继承这些酶的个体,出生后的生长速度会变慢,体长也会变短。翻译速度并非越快越好,通过添加糖来适当调控翻译速度,是生物健康生长的必要条件。
目前,研究团队正在制备缺失引起该修饰的基因小鼠模型,以便研究这些酶的功能。此前,已有实验结果显示,缺失QTGAL的小鼠表现出在明亮环境中活动时间减少的焦虑倾向,而缺失QTMAN的雌性小鼠的活动量则出现增加。此外,缺失QTMAN的小鼠会呈现肥胖体型,铃木教授的团队目前正在详细研究这些表型为何会因tRNA修饰缺失而产生。他表示:“这些酶可能与人类的疾病相关,比如精神疾病、癌症等,我们希望进一步阐明其中的关联。”
为治疗线粒体病带来新希望
开发使用纳米孔的全面检测技术
“操控”方向的研究也取得了初步成果。铃木团队发现,由线粒体DNA突变引发的“线粒体脑肌病(MELAS病)”患者,其tRNA未发生牛磺酸修饰,并且,在使用MELAS病患者细胞进行的实验中,成功恢复了tRNA的功能。
健康人群中,一种名为MTO1的酶会使tRNA的尿苷发生牛磺酸修饰。但在MELAS病患者中,由于tRNA中本应是腺嘌呤的碱基变成了鸟嘌呤,导致MTO1无法识别tRNA,尿苷无法发生牛磺酸修饰。铃木教授等通过过量表达MTO1使其在细胞内大量产生,成功恢复了tRNA的牛磺酸修饰,同时显著提升了细胞的蛋白质合成及呼吸活性(图5)。
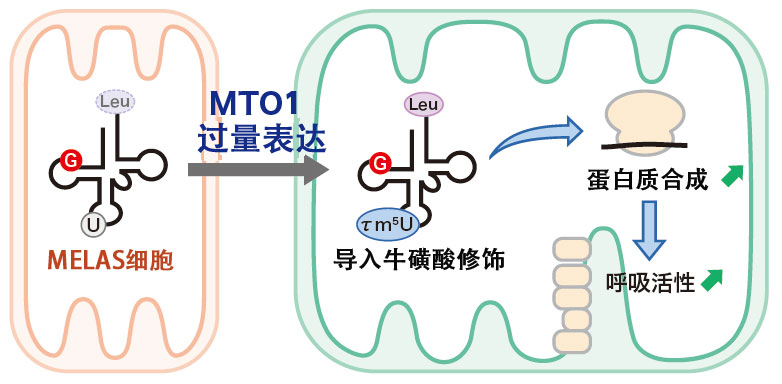
图5 铃木教授的团队通过过量表达MTO1,成功将本应存在的牛磺酸修饰(τm5U)导入tRNA,恢复了线粒体功能。亮氨酸(Leu)是构成蛋白质的20种氨基酸之一。
MELAS病是一种类似脑卒中发作的疑难病症,此前一直缺乏有效疗法,预后效果较差。铃木团队目前正与东京大学医科学研究所的冈田尚巳教授合作,研究使用腺相关病毒的MELAS病基因疗法,这一研究为难以通过基因组编辑治疗的线粒体病带来了新的治疗希望。
在进行上述研究的同时,铃木教授团队还在推进开发RNA修饰的检测技术。其中一项重要技术是使用名为“纳米孔测序仪”的装置进行tRNA修饰的单分子解析。在纳米孔测序仪解析中,将RNA拉伸成单链状态,使其通过由膜蛋白构成的被称为纳米孔的微孔,通过此时电流的变化来解析碱基序列。
铃木教授团队注意到,RNA修饰在通过纳米孔时会表现出特征性电流值。通过机器学习各tRNA通过时产生的特征性电流波形模式,不仅能解析碱基序列,还能在单分子水平上检测tRNA修饰的存在与否及修饰比例。全面检测tRNA修饰,将为阐明疾病成因、开展疾病诊断提供重要依据。
中心法则中RNA的作用,是高中教材中也会讲解的基础知识点。但教材中几乎未提及RNA修饰这一灵活的调控机制,也未介绍RNA修饰异常与疾病的关联,可以说,这是一个全新的研究领域。相信在本项目结束后,通过深入推进RNA修饰的研究,将进一步推动对生命现象的理解和医疗应用。(TEXT:岛田祥辅 PHOTO:上乐博之)

原文:JSTnews 2026年2月号
翻译:JST客观日本编辑部